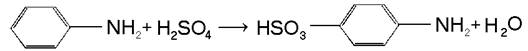.
Аминами называются органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородные радикалы ( предельные, непредельные, ароматические).
Название аминов производят от названия углеводородного радикала с добавлением окончания –амин
или от названия соответствующего углеводорода с приставкой амино-.
 Примеры:
Примеры:
CH3
– NH2
CH3
– NH – C2
H5
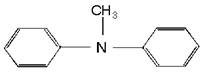
метиламин метилэтиламин мтилдифениламин
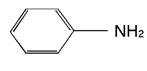
фениламин
(анилин)
В зависимости от числа атомов водорода, замещенных в аммиаке на углеводородные радикалы, различают первичные, вторичные и третичные
амины:
R
R- NH2
R – NH – R’ R – N – R”
первичный амин вторичный амин третичный амин
Где R, R’, R’’ – углеводородные радикалы.
Первичные, вторичные и третичные амины можно получить, проводя алкилирование (введение алкильного радикала) аммиака. При этом происходит постепенное замещение атомов водорода аммиака на радикалы, и образуется смесь аминов:
NH3
+ CH3
I --- CH3
NH2
+ HI
CH3
NH2
+ CH3
I --- (CH3
)2
NH + HI
(CH3
)2
NH + CH3
I --- (CH3
)2
N + HI
Обычно в смеси аминов преобладает один из них в зависимости от соотношения исходных веществ.
Для получения вторичных и третичных аминов можно использовать реакцию аминов с галогеналкилами:
(CH3
)2
NH + C2
H5
Br --- (CH3
)2
NC2
H5
+ HBr
Амины можно получить восстановлением нитросоединений. Обычно нитросоединения подвергают каталитическому гидрированию водородом:
C2
H5
NO2
+ 3H2
--- C2
H5
NH2
+ 2H2
O
Этот метод используется в промышленности для получения ароматических аминов .
Предельные амины. При обычных условиях метил амин CH3
NH2
, диметиламин (CH3
)2
NH, триметиламин (CH3
)3
N и этиламин C2
H5
NH2
– газы с запахом, напоминающим запах аммиака. Эти амины хорошо растворимы в воде. Более сложные амины – жидкости, высшие амины – твердые вещества.
Для аминов характерны реакции присоединения, в результате которых образуются алкиламиновые соли. Например, амины присоединяют галогеноводороды:
(CH3
)2
NH2
+HCl --- [(CH3
)2
NH3
]Cl
хлорид этиламмония
(CH3
)2
NH + HBr --- [(CH3
)2
NH2
]Br
бромид диметиламмония
(CH3
)3
N + HI --- [(CH3
)3
NH]I
иодид триметиламмония
Тритичные амины присоединяют галогенопроизводные углеводорода с образованием тетраалкиламмониевых солей, например:
(C2
H5
)3
N + C2
H5
I --- [(C2
H5
)4
N]I
Алкиламониевые соли растворимы в воде и в некоторых органических растворителях. При этом они диссоциируют на ионы:
[(C2
H5
)4
N]I === [(C2
H5
)4
N]+
+ I-
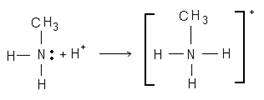
В результате водные и неводные растворы этих солей проводят электрический ток. Химическая связь в алкиламмониевых соединениях ковалентная, образованная по донорно-акцепторному механизму:
Ион метиламмония
Как и аммиак, в водных растворах амины проявляют свойства оснований. В их растворах появляются гидроксид-ионы за счет образования алкиламониевых оснований:
C2
H5
NH2
+ H2
O === [C2
H5
NH3
]+
+ OH-
Щелочную реакцию растворов аминов можно обнаружить при помощи индикаторов.
Амины горят на воздухе с выделением CO2
, азота и воды, например:
4(C2
H5
)2
NH + 27O2
--- 16CO2
+ 2N2
+ 22H2
O
Первичные, вторичные и третичные амины можно различить, используя азотную кислоту HNO2
. при взаимодействии этой кислоты с первичными аминами образуется спирт и выделяется азот:
CH3
– NH2
+ HNO2
--- CH3
– OH + N2
+H2
O
Вторичные амины дают азотистой кислотой нитрозосоединения, которые имеют характерный запах:
CH3
– NH2
– CH3 + HNO2
--- (CH3
)2
– N==NO+H2
O
Третичные амины не реагируют азотистой кислотой.
Анилин
C6
H5
NH2
является важнейшим ароматическим амином. Он представляет собой бесцветную маслянистую жидкость, которая кипит при температуре 184,4 0
С.
Анилин был впервые получен в XIX в. русским химиком-органиком Н. Н. Зининым, который использовал реакцию восстановления нитробензола сульфидом аммония (NH4
)2
S. В промышленности анилин получают каталитическим гидрированием нитробензола с использованием медного катализатора:
C6
H5
– NO2
+ 3H2
-cu
-- C6
H5
– NH2
+ 2H2
O
Старый способ восстановления нитробензола, который потерял промышленное значение, заключается в использовании в качестве восстановителя железа в присутствии кислоты.
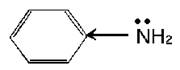 По химическим свойствам анилин во многом аналогичен предельным аминам, однако по сравнению с ними является более слабым основанием, что обусловлено влиянием бензольного кольца. Свободная электронная пора атома азота, с наличием которой связаны основные свойства, частично втягивается в П – электронную систему бензольного кольца:
По химическим свойствам анилин во многом аналогичен предельным аминам, однако по сравнению с ними является более слабым основанием, что обусловлено влиянием бензольного кольца. Свободная электронная пора атома азота, с наличием которой связаны основные свойства, частично втягивается в П – электронную систему бензольного кольца:
Уменьшение электронной плотности на атоме азота снижает основные свойства анилина. Анилин образует соли лишь с сильными кислотами. Например, с хлороводородной кислотой он образует хлорид фениламмония:
C6
H5
NH2
+ HCl --- [C6
H5
NH3
]Cl
Азотная кислота образует с анилином диазосоединения:
C6
H5
– NH2
+ NaNO2
+2HCl --- [C6
H5
– N+
==N]Cl-
+ NaCl + 2H2
O
Диазосоединения, особенно ароматические. Имеют большое значение в синтезе органических красителей.
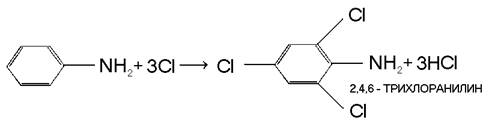
Некоторые особые свойства анилина обусловлены наличием в его молекуле ароматического ядра. Так, анилин легко взаимодействует в растворах с хлором и бромом, при этом происходит замещение атомов водорода в бензольном ядре, находящихся в орто
- и пара
-положенияхк аминогруппе:
Анилин сульфируется при нагревании с серной кислотой, при этом образуется сульфаниловая кислота:
Сульфаниловая кислота – важнейший промежуточный продукт при синтезе красителей и лекарственных препаратов.
Гидрированием анилина в присутствии катализаторов можно получить циклогексиламин:
C6
H5
– NH2
+ 3H2
--- C6
H11
– NH2
Анилин используется в химической промышленности для синтеза многих органических соединений, в том числе красителей и лекарств.
Другие работы по теме:
Традиционные способы очистки питьевой воды
Проблема обеспечения населения питьевой водой, отвечающей требованиям стандарта, является одной из основных задач, стоящих перед предприятиями и организациями водообеспечения России.
Реакции аминов
По рациональной номенклатуре амины - это алкил или ариламины. Алкилирование алкилгалогенидами и окисление третичных аминов. Ацилирование и действие сульфонилхлоридов, замещение ароматических аминов в кольцо. Взаимодействие аминов с азотистой кислотой.
Амины
Сущность, понятие и характеристика аминов. Их основные свойства и реакции. Характеристика реакций получения аминов, их восстановления и окисления. Методы получения аминов. Аммонолиз гелоленуглеводородов, описание их основных свойств и реакций соединений.
Амиды
Амидами называют производные кислот, в которых гидроксильная группа заменена на аминогруппу. Амиды могут быть получены из всех производных кислот. Реакции амидов: кислотность, восстановление, гидролиз, дегидратация, расщепление амидов по Гофману.
Ионно-парная хроматография
Сущность и содержание ионно-парной хроматографии, ее использование в жидкостной хроматографии и экстракции для извлечения лекарств и их метаболитов из биологических жидкостей в органическую фазу. Варианты ионно-парной хроматографии, отличительные черты.
Химия Шпаргалка
Азотосодержащ. в-ва. Нитросоединения, Амины, аминокислоты, белки. Амины. получение: R-NO2 +6H->R-NH2 +2H20 (нитросоед.) (амин) первичные: H-N-CH3 (метиламин)
Синтез бензальанилина
Методы синтеза и химические свойства аминов. Изомерия в ряду алифатических аминов и восстановление нитросоединений. Получение первичных, вторичных ароматических аминов. Получение третичных аминов. Реагенты и оборудование и синтез бензальанилина.
Нитросоединения
Сущность и понятие нитросоединений. Способы их получения и реакция нитросоединения. Таутомерия алифатических нитросоединений и конденсация их с альдегидами и кетонами. Восстановление и окисление нитросоединений. Реакции получения соединений, их описание.
Биогенные амины и алкалоиды
Понятие гликозидов, их классификация и разновидности, значение и характер воздействия на организм, распространенность и основные функции. Биогенные амины и алкалоиды как антиалиментарные факторы. Характеристика основных алкалоидов - морфина и кофеина.
Алифатические амины
Понятие аминов, их сущность и особенности, общая формула и основные химические свойства. Классификация аминов на ароматические и алифатические, их отличительные черты. Особенности алифатических аминов, способы их получения и характерные реакции.
Химия (Шпаргалка)
Азотосодержащ. в-ва. Нитросоединения, Амины, аминокислоты, белки. Амины. получение: R-NO +6H->R-NH (нитросоед.) (амин) первичные: H-N-CH (метиламин)
Реакции С и О ацилирования
Введение. Реакции ацилирования обладают очень многими полезными свойствами. Они позволяют вести в молекулу функциональную группу C=O путем реакций присоединения либо замещения, не подвергая исходную молекулу окислению (восстановлению). Таким образом, можно получать соединения различных классов: а) амиды; б) сложные эфиры; в) ангидриды карбоновых кислот; г) кетоны и другие полезные соединения.
Аминокислоты 2
Содержание: Введение Классификация аминокислот Виды изомерии аминокислот Двухосновные моноаминокислоты Одноосновные диаминокислоты Оксиаминокислоты
Ненасыщенные спирты Фенолы Хиноны
К ненасыщенным относятся спирты с двойной углерод-углеродной связью (1,2); с тройной углерод-углеродной связью (3); фенолы (4). Спирты с двойной углерод-углеродной связью бывают винильного (CH2=CH-OH) и аллильного типа (CH2=CH-CH2-OH; CH2=CHCH2CH2OH).
Методы органического синтеза
Органический синтез как раздел химии, предмет и методы его изучения. Сущность процессов алкилирования и ацилирования, характерные реакции и принципы протекания. Описание реакций конденсации. Характеристика, значение реакций нитрования, галогенирования.
Синтез, свойства и применение дифениламина. Амины и их свойства
Применение дифениламина. Амины. Ацилирование и алкилирование аминов. Образование производных мочевины. Алкилирование первичных и вторичных аминов. Расщепление и окисление аминов. Синтез на основе анилина и анилиновой соли. Синтез из хлорбензола и анилина.
Синтез и свойства амилнитрита
Амилнитрит, как противоядие при отравлениях. Проблема нитратов и нитритов. Методика синтеза. Неорганические и органические нитриты. Способы получения нитросоединений. Реакции нитросоединений. Амины. Диазо- и азосоединения. Реакции солей арилдиазония.
Кислотность и основность по Бренстеду-Лоури
Понятие кислот по Бренстеду, способных отдавать протон, а оснований - его присоединяющих. Химизм кислотно-основных взаимодействий растворения серной кислоты в воде, способность к автопротолизу. Константа основности в оценке кислотности растворов.
Еноляты лития. Конденсации Клайзена и Дикмана
Обратимая реакция Образования енолятов при действии оснований на альдегиды и кетоны. Получение диизопропиламида лития. Механизм сложноэфирной конденсации Клайзена и Дикмана. Реакции Перкина и Манниха. Получение енаминов, их ацилирование по двойной связи.
Трава череды трехраздельной
Фармакологические свойства череды трехраздельной. Сбор и сушка сырья. Общая информация о череде трехраздельной. Применение растения в медицине. Основные вещества череды трехраздельной. Лекарственные формы, способ применения и дозы. Настой травы череды.
Неотложная помощь и лечение поствакцинальных осложнений
Тяжелые поствакцинальные реакции являются достаточно редкими, но не настолько, что бы их не принимать во внимание. По статистике США: 50 детей ежегодно остаются с неустранимыми изменениями со стороны ЦНС, возникшими после вакцинации.
Радиопротекторы 3
МИНИСТЕРСТВО ОБРАЗОВАНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ УО «БЕЛОРУССКИЙ ГОСУДАРСТВЕННЫЙ ЭКОНОМИЧЕСКИЙ УНИВЕРСИТЕТ» Кафедра «Товароведение непродовольственных товаров»
Реакция Габриеля
Синтез первичных аминов алкилированием фталимида К алкилгалогенидами с последующим расщеплением образующегося N-замещенного фталимида.
Спорынья
Спорынья—ядовитый паразитный гриб из класса сумчатых гибов семейства спорыньевых. Известны 9 видов спорыньи, паразитирующих на злаках: ржи, ячмене, пшенице, овсе, пырее, овсянице, еже, тимофеевке, костре и др.
Расторопша пятнистая (остро-пестро)
Расторопша пятнистая — однолетнее травянистое растение семейства сложноцветных, достигающее в высоту 60—150 см. Стебель голый или слабо паутинисто-опушенный, бороздчатый, ветвистый.
Каучук
В конце 20-х годов нашего столетия ленинградские химики во главе с С. В. Лебедевым разработали способ получения каучука из этилового спирта с последующей полимеризацией его на металлическом натрии.
Радиопротекторы
План реферата. Введение Глава 1. Общая характеристика радиопротекторов. Пути поиска новых веществ. Глава 2. Характеристика отдельных радиопротекторов.
Радиопротекторы
План реферата. Введение Глава 1. Общая характеристика радиопротекторов. Пути поиска новых веществ. Глава 2. Характеристика отдельных радиопротекторов.
 Примеры:
Примеры:
 По химическим свойствам анилин во многом аналогичен предельным аминам, однако по сравнению с ними является более слабым основанием, что обусловлено влиянием бензольного кольца. Свободная электронная пора атома азота, с наличием которой связаны основные свойства, частично втягивается в П – электронную систему бензольного кольца:
По химическим свойствам анилин во многом аналогичен предельным аминам, однако по сравнению с ними является более слабым основанием, что обусловлено влиянием бензольного кольца. Свободная электронная пора атома азота, с наличием которой связаны основные свойства, частично втягивается в П – электронную систему бензольного кольца: