На тему: «Загадочная вода».
Ученик 8с класса КРФМЛИ
Туркин Евгений.
г. Сыктывкар.
2003 г.
Какие изменения происходят в воде, при изменении внешних условий, в чём они появляются, и почему так происходит? Знать это одинаково важно и для геолога, и для астонома, и для биолога. В природе нет более распространённого вещества, чем вода.
Вода течёт реками, разливается озёрами, сгущается тучами в небе, стелится туманом по земле. Она зримо и не зримо присутствует всюду.
Почти 200 лет уже исследуют учёные воду, но свойства её рас -крыты и объяснены ещё не полностью. Пожалуй, ни одно вещество при его изучении не вело себя так загадочно. Бессчётное количество раз поведение её, казалось, шло вразрез со всеми законами физики.
В 18 веке учёные решили, что частица воды состоит из одного атома водорода и одного атома кислорода. И сразу столкнулись с загадкой. При соединении одного объёма кислорода с двумя объё -мами кислорода неизменно возникло два объёма воды, а не один. Почему? Ведь если в равных объёмах газов содержится равные ко -личества частиц, и частицы не делятся.… Не менее странным каза -лось и то, что водяной пар, состоящий из кислорода и водорода, легче кислорода, своей части.
Около 75 лет ушло на то, чтобы примирить теорию с практикой. Как только было доказано, что химическая формула воды Н2О, а не НО, всё сразу стало на свои места.
При соединении двух объёмов водорода с одним стало получаться два объёма воды: 2Н2+О2=2Н2О.
Просто объяснялась и непонятная прежде лёгкость водяного пара. В самом деле: молекула воды входит только один атом кислорода, а в молекуле кислорода их два. Вес водорода в воде можно не учи -тывать, потому что атом водорода в 16 раз легче атома кислорода.
Но на этом все неприятности с водой не закончились, просто она стала вести себя менее загадочно. Поведение её с точки зрения физики и химии по-прежнему не вписывалось не в какие рамки. Учёным никак не удавалось понять, от чего для нагревания воды надо затратить гораздо больше энергии, чем для нагревания такого же количества, скажем, железа или песка. Почему вода кипит при 100º ,а замерзает при 0º.
Для химиков таблица Менделеева – всё равно что адресное бюро для человека, приехавшего в незнакомый город. Она помогает бы -стро ориентироваться. Достаточно знать, какое место занимает химический элемент в таблице, чтобы тут же получить о нём почти все сведения.
Воды, конечно в таблице Менделеева нет, но там есть кислород (О). Он стоит в одной группе с теллуром (Те), серой (S) и селеном (Sе). Прописка элементов в одной группе говорит о том, что соединения с водородом одинаковы. Каждый из атомов этих эле -ментов соединяется с двумя атомами водорода. В результате воз -никают: вода (Н2О), сероводород (Н2S), селенистый водород (Н2Sе) и теллуристый водород (Н2Sе). Молекула воды самая лёгкая из них. Она тяжелее атома водорода всего в 18 раз. Молекулярный вес теллуристого водорода – 130 – он самый тяжёлый.
Естественно чем тяжелее молекулы, тем больше должны быть си -лы, которые притягивают их друг к другу. Не будь так, все тела попросту распались бы. Чем больше силы взаимного притяжения молекул, тем более бурным должно быть их хаотическое движение для того, чтобы они могли разорвать свои связи и вещество зак -ипело. Чем оно интенсивнее, тем температура выше. Значит чем тяжелее вещество, тем при более высокой температуре оно будет кипеть. Теллуристый водород начинает кипеть при -4°С. Селенис - тый водород легче, поэтому точка кипения лежит ниже, она -42°С. Сероводород кипит при –61°С. Тогда вода, как самое лёгкое из них, должна кипеть ещё при более низкой температуре. Но однако, она кипит при 100°С, это знают все.
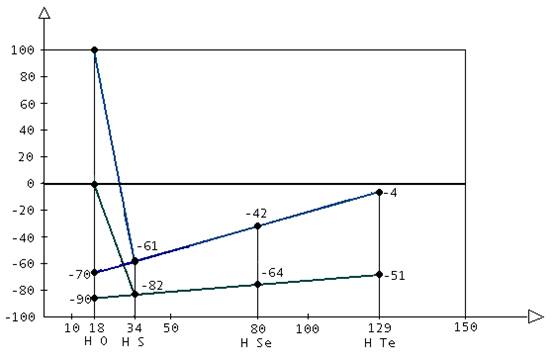
Если соединить нанесённые точки кипения Н2Те, Н2Sе, Н2S, получится почти прямая линия. Казалось бы, точка кипения воды должна лежать на её продолжении. Но она вдруг резко прыгает вверх, к 100°С. Та же странность происходит и при замерзании воды. По графику она должна была бы замерзнуть лишь при –90°С, между тем она превращается в лёд при 0°С.
Разве может вода не подчинятся общим для других веществ физико-химическим законам? Значит, в мире молекул действуют какие-то неизвестные, а может быть, и не правильно понятые силы?
Объяснить, почему вода кипит при 100°С, а замерзает при 0°С, удалось лишь около 70 лет тому назад. Дело в том, что одна сторона их имеет положительный заряд, а другая – отрицательный. Про такие молекуле говорят, что они полярны. Полярность молекул вызвана тем, что атомы водорода присоединяются к атому кисло –рода не симметрично с боков, а в молекуле сероводорода или теллуристого водорода, а тяготеют к одной стороне.
Как только водород соединится с кислородом, тот час орбиты его электронов меняются, отклоняясь к кислороду. Ведь электроны водорода принадлежат теперь не ему одному, они стали общим достоянием водорода и кислорода. Но из-за изменения орбиты электронов ядра водорода, обладающие положительным зарядом, обнажаются. В целом молекула воды, конечно, остаётся нейтральной. Но та сторона её, где присоединился водород, оказывается положительной по заряду, а та, куда сдвинулись электроны, - отрицательна.
Из-за того, что молекулы воды полярны, между ними кроме обычных сил притяжения действуют ещё и электрические. Они получили названия водородных связей. Одна молекула воды может удержать ими возле себя целых 4 молекулы. Вот почему вода кипит не при –70°С, а при 100°С, и замерзает при температуре на 90° выше, чем ей полагалось бы.
Водородные связи делают воду чудесной, непохожей ни на какую другую, жидкость. Количество тепла, нужное для нагревания одного грамма её на один градус, иными словами теплоёмкость, в два раза больше, чем теплоёмкость спирта, в 30 – чем ртути. Способность воды запасать в себе, словно печка, большие количества тепла, а затем отдавать его обратно имеет огромное значение для жизни Земли. В тех местах, где её поблизости нет, разница между ночной и дневной температурами достигает 50°. При таком перепаде температур лопаются камни! В знойной Сахаре после испепе –ляющей жары, ночью без костра можно замёрзнуть! Оберегая растения от заморозков, садовники ставили в неотапливаемых оранжереях бочки с водой. Остывая на 10°, бочка давала столько же тепла, сколько небольшая охапка дров.
Для того чтобы нагреть 1 литр воды от 0° до 100°, надо затратить 100 кило калорий. Для того чтобы испарить тот же литр, - в 5 раз больше. Вот почему так холодно в мокром костюме. Удивительные свойства воды неисчислимы. Она вовсе не такая мягкая и под –датливая, как кажется. Об неё можно больно ушибится если неудачно нырнёшь. Столкновение дождинки с реактивным самолётом оставляет след на его корпусе. В США есть токарный станок, где вода режет бетон. Кажется невероятным, но вода прочна, как сталь.
Вода универсальный растворитель. В природе нет, ни одного вещества, которое бы не растворялось в тех или иных количествах. Тончайшие аналитические весы показали бы, что вместе со стаканом чая вы каждый день выпиваете 0,0001 грамма растворённого стекла.
Абсолютно чистой воды в природы нет. Не получена она пока ещё ни в одной лабораторий.
Вода чутко реагирует на любые изменения внешних условий: на давление, на температуру. Её свойства изменяются на некоторое время даже после того, как она побывает обычным льдом. Урожай пшеницы и кукурузы, если их поливать водой из растаявшего льда, возрастает в 1,5 раза. Молодые животные на такой воде быстрее растут. Недаром биологи называют её иногда «живой» водою. Благотворно действует на растения и вода, прошедшая через магнитное поле. В чём тут дело, пока не разгадано.
Вода «знает» не только о земных делах, она поддерживает каким-то образом самую тесную связь с космосом. Давно известно, что скорость протекания одной и той же химической реакции в разное
время бывает неодинаковой. Словно вода прислушивалась к какому-то зову из космоса и, послушная ему, несколько меняла свои свойства. По всей вероятности, так оно и есть, – на поведение воды влияют события на Солнце. Как это происходит и в чём выражается, пока ещё учёные не знают.
Вода и в наши дни так же загадочна как 200 лет назад.
Другие работы по теме:
Некоторые вопросы экологии
Роль грибов в биоценозе леса, их значение в процессах разложения и минерализации подстилки и лесного опада, участие в круговороте веществ. Функции листа Покрытосеменных. Практические результаты исследования качества воды из-под крана и после кипячения.
Питьевая вода
Вода является основной средой, в которой протекают многочисленные химические реакции и физико-химические процессы обмена веществ. Организм строго регулирует содержание воды в каждом органе, каждой ткани.
Вода в грунті
Реферат на тему: “” 1. Функції води в природі та житті ґрунту Вода в природі виконує дві функції: забезпечує багато фізичних і хімічних процесів; є потужною транспортною геохімічною системою, яка сприяє переміщенню речовин у просторі. У житті ґрунту вода виконує п’ять функцій: вона є одним з факторів ґрунтоутворення й процесів вивітрювання мінералів; гумусоутворення, хімічні реакції відбуваються тільки у водному середовищі; під впливом води проходить формування ґрунтового профілю; регулювання температури грунту відбувається при допомозі води; вода є одним із факторів життя рослин та організмів, а також родючості грунтів.
Вода в жизнедеятельности человека
Вода выступает необходимым показателем существования всех живых организмов на Земле. Окажись вы в пустыне под ее беспощадно палящим солнцем, вы будите счастливы променять пусть не все, но некоторые ценности на воду, на хотя бы один глоток этого живительного и бесценного «жидкого золота». Бедуины имели представление о том, что никакие богатства не спасут путника в пустыне, в том случае если иссякнут запасы воды.
Гидролиз
Гидролизом называется обменная реакция вещества с водой, в результате которой образуются малорастворимые или малодиссоциированные соединения (основания, кислоты, основные соли). Вода является амфотерным электролитом, т. е. она может взаимодействовать и как кислота, и как основание. В первом случае связываются водородные ионы, во втором – гидроксильные ионы.
Вода 3
Вода оксид водорода – наиболее распространённое нашей планеты и важное. Водная оболочка Земли, гидросфера, содержит около 1,5 млрд. км3. В земной коре, литосфере, в связанном состоянии находится 1,4 млрд. км3. В атмосфере – 15 тыс. км3. поверхность Земли, занятая водой, в 2 с половиной раза больше суши.
Доказательства
Индуктивное косвенное доказательство. Дедуктивное косвенное доказательство. Прямые доказательства. Ошибка тезиса, аргумента и демонстрации.
Подбор состава тяжелого бетона
Водоцементное отношение После преобразования относительно В/Ц эта формула примет вид: А=0,55 - для материалов пониженного качества Расход воды на 1 м
Табличные значения наиболее распространенных жидкостей
П.В.Скулов, Физический факультет БГПУ В таблице приведены значения:плотность, удельная теплоемкость, удельная теплота плавления, удельная теплота парообразования,температура плавления, температура кипения, коэффициент поверхностного натяжения, динамическая вязкость, скорость распространения звука.
Сочинения на свободную тему - Аквариум деловое описание 1
Аквариум - это стеклянная емкость с водой для содержания рыб и растений. Аквариумы бывают разной формы: круглые, прямоугольные, сферические. У меня дома прямоугольный аквариум. Он стоит возле стены, примыкающей к окну. Это самое лучшее место для него, потому что нет яркого солнечного света, от которого вода быстро испаряется и начинает цвести.
Шолохов м. а. - Враги народа по роману м. шолохова
Еще не до конца разгадана тайна бессмертия великих творений человеческого разума и сердца. По прежнему зачарованно смотрит мир на улыбку. Джаконды по прежнему манит за собой загадочная незнакомка по прежнему спорят критики о том осуждает ли Шолохов св Яков Лукич Островное по природе своей умный человек любящий и умеющий трудиться.
Топливо
Топливный цикл. Теплоносители реакторов. Замедлители реакторов.
Осторожно! Живая вода
Исследования метастабильного состояния водных растворов, полученных посредством электрохимической обработки, положили начало способу обработки жидкостей – электрохимической активации.
Чайка на крижині
Автор: Костенко Ліна. В цьому році зима не вдягала білої свити. Часом вже й приміряла, та хтось її зразу крав. Пошукала, поплакала... Що ж робити? -- Бідувала в старій із торішніх зів"ялих трав.
Ой у степу криниченька
Автор: Народна творчість. Ой у степу криниченька, З неї вода протікає. Гей, там чумак сиві воли пасе Та з криниці напуває. Воли ревуть, води не п'ють. Бо в Крим доріженьку чують.
Черная вода
Автор: Хармс Д. Андрей Иванович плюнул в чашку с водой. Вода сразу почернела. Андрей Иванович сощурил глаза и пристально посмотрел в чашку. Вода была очень черна. У Андрея Ивановича забилось сердце. В это время проснулась собака Андрея Ивановича. Андрей Иванович подошел к окну и задумался. Вдруг что-то большое и темное пронеслось мимо Андрея Ивановича и вылетело в окно.
Письмо Софье Павловне Фамусовой
Автор: Грибоедов А.С. Здравствуйте, уважаемая Софья Павловна! Прежде, чем написать Вам письмо, я долго раздумывал над этим. И окончательно сделал для себя вывод, что я должен был его написать.
Письмо Софье Павловне Фамусовой 2
Письмо Софье Павловне Фамусовой Автор: Грибоедов А.С. Здравствуйте, уважаемая Софья Павловна! Я давно хотел написать вам это письмо, но всё никак не решался. И наконец, после долгих раздумий, окончательно сделал для себя вывод, что я должен был его написать. Хотелось бы Вам сказать, что после прочтения ваших предыдущих писем, адресованных мне, я понял лишь то, что вы очень загадочная и весьма непредсказуемая молодая особа.
Сочинение-описание трудовых процессов. Как получают сахар.
Автор: Сочинения на свободную тему На летние каникулы я приехала к бабушке в деревню. Как-то вечером я сидела за столом и ела яблоко. Ко мне подошел мой дедушка, и я спросила: «А почему яблоко сладкое?». Он ответил: «Очень просто: в нем есть сахар. Сахар есть во всех фруктах и овощах, даже в горьком хрене. Свекла слаще яблока – в ней очень много сахару.
Враги народа в романе М. Шолохова “Поднятая целина”
По-прежнему зачарованно смотрит мир на улыбку Джоконды, по-прежнему манит за собой загадочная “незнакомка”, по-прежнему спорят критики о том, осуждает ли Шолохов своего Григория Мелехова или сочувствует ему.
Весна в лесу
Автор: Сочинения на свободную тему "Еще в полях белеет снег, А воды уж весной шумят - Бегут и будят сонный брег, Бегут, и блещут, и гласят..." Ф.Тютчев
Гейзер
Есть на свете удивительные фонтаны, они действуют сами по себе, без участия человека. Вода в них горячая — кипяток. Бьют они прямо из-под земли на десятки метров вверх. Это гейзеры.
Вода
Запасы, свойства, кислотно-основные свойства.
Вода
Функции воды. Свойства воды.
Целебные свойства талой воды
Издавна считалось, что употребление талой воды способствует омоложению организма. Талая вода отличается от обычной своей структурой, более сходной со структурой протоплазмы наших клеток.
Табличные значения наиболее распространенных жидкостей
В таблице приведены значения:плотность, удельная теплоемкость, удельная теплота плавления, удельная теплота парообразования,температура плавления, температура кипения, коэффициент поверхностного натяжения, динамическая вязкость.
Предельные углеводороды 2
МИНОБРНАУКИ РОССИИ Пыть-Яхский индустриальный колледж . Образовательного учреждения высшего образования «ЮГУ» Специальность:151031 Лабораторная работа № 7
Понижение жесткости воды вымораживанием
Для успешного разведения многих видов рыб совершенно необходима мягкая вода. Так как аквариумист-любитель почти никогда не может достать подходящую по качеству воду из естественных водоемов, он вынужден сам заниматься снижением жесткости воды.
Джеймс Хопвуд Джинс
Английский физик и астроном Джеймс Хопвуд Джинс родился в Лондо- не. В 1900 г. он окончил Кембрджский университет и в течении ряда лет преподавал там математику . Астрономические работы Джинса посвящены проблеме строения и эволюции звезд.
Хуан Руис , архипресвитер из Иты
Хуан Руис (род.ок.1283г. -ум.ок.1350г.), известный также как архипресвитер из Иты, фигура во многом загадочная. Всё, что о нём известно, извлечено из его же собственного произведения - "Книги благой любви" (Libro de buen amor).
Живая и мертвая вода - коротко
Реферат по теме: Живая и мертвая вода”. Ученика 11 класса “Ю” “... На пути из Гаэты в Неаполь галера “Санта Лука” шла под парусами при свежем ветре. Находяс почти в 2х милях от Порты она остановилась почти неподвижно, несмотря на то, что все паруса были подняты. После осмотра руля и других частей корабля оказалось, что все в порядке, тогда матросы стали грести.
Забруднення водойм
Проблеми питної води. Вода становить майже 70% маси нашого організму. Втрата її організмом дуже небезпечна. Без води різко погіршується обмін речовин, що загрожує всім життєвим процесам. Без їжі людина може прожити понад місяць, без води вона гине через кілька днів.