Валериановые
кислоты С4Н9СООН, мол. м. 102,13. В статье рассмотрены кислоты, содержащие
бутильный остаток, связанный с группой СООН.
Валериановая
(пентановая) к-та СН3(СН2)3СООН (В.к.) - бесцв. жидкость; т. пл. -34,5°С, т.
кип. 185,4°С, 93,5-94°С/21 мм рт. ст.; d420 0,9459, nD20 1,41.00;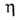 2,359 мПа*с (15°С);
2,359 мПа*с (15°С); Hoобр
- 548,9 кДж/моль,
Hoобр
- 548,9 кДж/моль,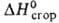 -2853,4 кДж/моль; К 1,147*10-5 (20°С); р-римость в воде 4,97% (25 °С). Образует
бинарные азеотропные смеси с многими в-вами, напр. с бромбензолом (3,5% В.к.;
т. кип. 155,6°С). Соли и эфиры В. к. наз. валератами. Содержится в продуктах
перегонки древесины, бурого угля и др. В пром-сти получают гидроформилированием
1-бутена с послед. окислением образующегося альдегида; окислением амилового
спирта. Наряду с бутилвалератом получается при обработке бутанола СО в присут.
NiI2 и Nal или никеля Ренея в водном р-ре при 340 °С и 37,5 МПа. Эфиры В. к.,
обладающие фруктовым и цветочным запахом (напр., изомилвалерат), -
ароматизирующие в-ва для пищ. продуктов, душистые в-ва в парфюмерии; используют
также как р-рители, сырье в произ-ве лек. в-в.
-2853,4 кДж/моль; К 1,147*10-5 (20°С); р-римость в воде 4,97% (25 °С). Образует
бинарные азеотропные смеси с многими в-вами, напр. с бромбензолом (3,5% В.к.;
т. кип. 155,6°С). Соли и эфиры В. к. наз. валератами. Содержится в продуктах
перегонки древесины, бурого угля и др. В пром-сти получают гидроформилированием
1-бутена с послед. окислением образующегося альдегида; окислением амилового
спирта. Наряду с бутилвалератом получается при обработке бутанола СО в присут.
NiI2 и Nal или никеля Ренея в водном р-ре при 340 °С и 37,5 МПа. Эфиры В. к.,
обладающие фруктовым и цветочным запахом (напр., изомилвалерат), -
ароматизирующие в-ва для пищ. продуктов, душистые в-ва в парфюмерии; используют
также как р-рители, сырье в произ-ве лек. в-в.
Изовалериановая
(3-метилбутановая, (5-метилмасляная) к-та (СН3)2СНСН2СООН (И.к.)-бесцв.
жидкость; т. пл. -29,3°С, т. кип. 176,5°С, 99,5°С/37 мм рт. ст.; d415 0,9308,
nD15 1,4030;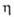 2,731
МПа*с (15°С);
2,731
МПа*с (15°С);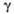 0,024
Н/м (30 °С);
0,024
Н/м (30 °С);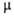 3,03*10-30 Кл*м;
3,03*10-30 Кл*м;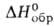 -561,5 кДж/моль,
-561,5 кДж/моль, - 2840,8 кДж/моль; К 1,216*10-5 (60°С); раств. в воде (4,2 г в 100 мл),
этаноле, эфире, хлороформе. Соли и эфиры И.к. наз. изовалератами, напр.
этилизовалерат (т. пл. 134,1°С; d420 0,8656, nD20 1,3692; р-римость в воде
0,17%; содержится в ананасах), изоамилизовалерат (жидкость; т. кип. 73-76°С/14
мм рт. ст.; d420 0,8812, nD20 1,4108; в воде раств. плохо).
- 2840,8 кДж/моль; К 1,216*10-5 (60°С); раств. в воде (4,2 г в 100 мл),
этаноле, эфире, хлороформе. Соли и эфиры И.к. наз. изовалератами, напр.
этилизовалерат (т. пл. 134,1°С; d420 0,8656, nD20 1,3692; р-римость в воде
0,17%; содержится в ананасах), изоамилизовалерат (жидкость; т. кип. 73-76°С/14
мм рт. ст.; d420 0,8812, nD20 1,4108; в воде раств. плохо).
И.к.
содержится в корне валерианы лекарственной, из к-рого ее и получают отгонкой с
водяным паром, а также в чайном листе, эфирных маслах нек-рых цитрусовых и др.
Синтезируют ее окислением изоамилового спирта, напр.: электролитич. способом в
р-ре H2SO4 с добавкой MnSO4 на аноде, изготовленном из РbО2, при 20°С; при
нагр. на воздухе с NaOH + КОН (в соотношении 2:1) и небольшим кол-вом Н2О при
285-295°С или с NaOH в присут. основного карбоната меди CuCO3*Cu(OH)2*0,5Н2О
при 140°С. Вместе с пивалиновой к-той получается карбонилированием изобутилена
при 250°С и 20 МПа [кат. - Ni(СО)4 и NiI2]. И.к. применяют в произ-ве валидола,
бромизовала, корвалола, валокордина и др. лек. в-в, фруктовых эссенций и
душистых в-в в парфюмерии.
Метилэтилуксусная
(2-метилбутановая, метилмасляная)
к-та СН3СН2СН(СН3)СООН (М.к.) - бесцв. жидкость, оптически активна.
(+)-Изомер-т. кип. 86,5-87,5°С/26 мм рт. ст.;d425 0,9313, nD20 1,4058;
метилмасляная)
к-та СН3СН2СН(СН3)СООН (М.к.) - бесцв. жидкость, оптически активна.
(+)-Изомер-т. кип. 86,5-87,5°С/26 мм рт. ст.;d425 0,9313, nD20 1,4058; + 35,56° (неразбавленная к-та). Получают (+ ) - M. к. расщеплением рацемата с
помощью цинхонидина. Содержится в эфирных маслах, напр. лавандовом. (-)-Изомер
- т. кип. 71-72°С/12 мм рт. ст., 64°С/2мм рт. ст; d425 0,9340, nD25 1,4038;
+ 35,56° (неразбавленная к-та). Получают (+ ) - M. к. расщеплением рацемата с
помощью цинхонидина. Содержится в эфирных маслах, напр. лавандовом. (-)-Изомер
- т. кип. 71-72°С/12 мм рт. ст., 64°С/2мм рт. ст; d425 0,9340, nD25 1,4038;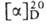 —24° (водный р-р; концентрация 0,9 мг/л). Синтезируют (—) - М. к. окислением
2-метил-1-бутанола действием КМnО4 в водно-щелочном р-ре или К2Сr2О7 в среде
H2SO4. При окислении (— )-изомера М. к. действием КМnО4 в водно-щелочном р-ре
получается 2-ги-дрокси-2-метилмасляная к-та. Рацемат М. к.-т. пл. — 48 оС, т.
кип. 176,5°С, 88°С/20мм рт. ст.; d420 0,9361, nD20 1,4060;
—24° (водный р-р; концентрация 0,9 мг/л). Синтезируют (—) - М. к. окислением
2-метил-1-бутанола действием КМnО4 в водно-щелочном р-ре или К2Сr2О7 в среде
H2SO4. При окислении (— )-изомера М. к. действием КМnО4 в водно-щелочном р-ре
получается 2-ги-дрокси-2-метилмасляная к-та. Рацемат М. к.-т. пл. — 48 оС, т.
кип. 176,5°С, 88°С/20мм рт. ст.; d420 0,9361, nD20 1,4060;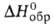 -557,3 кДж/моль,
-557,3 кДж/моль,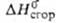 -2845
кДж/моль. Синтезируют декарбоксилированием метилэтилмалоновой к-ты,
карбонилированием втор-бутанола действием Ni(CO)4 в присут. NiCl2 и соляной
к-ты при 300 °С и 4 МПа или пропусканием смеси втор-бутанола и СО над NiI2 на
силикагеле при 230°С и 21 МПа, а также гидрокарбонилированием 1-бутена в разб.
уксусной к-те в присут. Ni(CO)4 (при этом образуется и валериановая к-та).
Применяется рацемич. М.к. в произ-ве пластификаторов, синтетич. смазок, лек.
в-в, как экстрагент меркаптанов из углеводородов и стабилизатор виниловых
полимеров.
-2845
кДж/моль. Синтезируют декарбоксилированием метилэтилмалоновой к-ты,
карбонилированием втор-бутанола действием Ni(CO)4 в присут. NiCl2 и соляной
к-ты при 300 °С и 4 МПа или пропусканием смеси втор-бутанола и СО над NiI2 на
силикагеле при 230°С и 21 МПа, а также гидрокарбонилированием 1-бутена в разб.
уксусной к-те в присут. Ni(CO)4 (при этом образуется и валериановая к-та).
Применяется рацемич. М.к. в произ-ве пластификаторов, синтетич. смазок, лек.
в-в, как экстрагент меркаптанов из углеводородов и стабилизатор виниловых
полимеров.
Пивалиновая
(триметилуксусная, неопентановая) к-та (СН3)3ССООН (П.к.)-т. пл. 35,7°С, т.
кип. 164,15°С, 77-78°С/20мм рт.ст.; d2040 0,905, nD25 1,4030;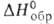 - 565,7 кДж/моль,
- 565,7 кДж/моль,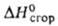 - 2836,6 кДж/моль;
- 2836,6 кДж/моль;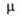 5,7*10-30 Кл*м; К 0,732*10-5 (60°С); р-римость в 100 г воды 2,2 г (20°С). Р-ции
П. к. осложнены стерич. препятствиями, связанными с экранированием
карбоксильной группы СН3-группами. Напр., П. к. труднее этерифицируется, чем
другие В.к.; эфиры ее более устойчивы при гидролизе и окислении. При окислении
Н2О2 в присут. FeSO4 в водном р-ре H2SO4 П. к. превращается в
2,2,5,5-тетраметиладипиновую к-ту НООСС(СН3)2СН2СН2С(СН3)2СООН, хлорируется при
облучении УФ-светом (
5,7*10-30 Кл*м; К 0,732*10-5 (60°С); р-римость в 100 г воды 2,2 г (20°С). Р-ции
П. к. осложнены стерич. препятствиями, связанными с экранированием
карбоксильной группы СН3-группами. Напр., П. к. труднее этерифицируется, чем
другие В.к.; эфиры ее более устойчивы при гидролизе и окислении. При окислении
Н2О2 в присут. FeSO4 в водном р-ре H2SO4 П. к. превращается в
2,2,5,5-тетраметиладипиновую к-ту НООСС(СН3)2СН2СН2С(СН3)2СООН, хлорируется при
облучении УФ-светом (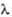 =
365,5 нм) в 3-хлор-2,2-диметилпропионовую к-ту С1СН2С(СН3)2СООН, при взаимод. с
РС13, РС15, SOC12 или СОС12 образуется пивалоилхлорид. Соли и эфиры П. к. наз.
пивалатами, напр. этилпивалат (т. пл. 89,5 °С, т. кип. 119°С).
=
365,5 нм) в 3-хлор-2,2-диметилпропионовую к-ту С1СН2С(СН3)2СООН, при взаимод. с
РС13, РС15, SOC12 или СОС12 образуется пивалоилхлорид. Соли и эфиры П. к. наз.
пивалатами, напр. этилпивалат (т. пл. 89,5 °С, т. кип. 119°С).
В
пром-сти П. к. получают карбонилированием изобутилена в присут. HF и Н2О при
40-60°С и 5 МПа; выход 95%. С хорошими выходами м. б. синтезирована таким же
способом из бутанола или трет-бутанола (кат. - НВF4*Н2О) в среде H2SO4. П. к.
применяют в произ-ве лек. в-в, теплостойких смазок, гербицидов и аттрактантов;
к-та и ее Li-соль повышают октановое число моторных топлив. Для защиты
древесины м. б. использован пивалат Sn. Эфиры П. к. с бутиловыми спиртами -
ароматизирующие в-ва для пищ. продуктов (фруктовый, цветочный или винный
запах), эфиры с полиолами-пластификаторы.
Список литературы
Ullmans
Encyklopadie, 4 Aufl., Bd9,Weinheim, 1975, S. 142-44: Kirk-Othmer encyclopedia,
3 ed., v. 4, N. Y.-[a.o.J, 1978, p. 864-71.
Другие работы по теме:
Кислотные осадки
Дождь, снег или дождь со снегом, имеющие повышенную кислотность. Кислотные осадки возникают главным образом из-за выбросов оксидов серы и азота в атмосферу при сжигании ископаемого топлива (угля, нефти и природного газа).
Промышленное получение азотной кислоты
Варнавский 9в Промышленное получение азотной кислоты. Окисление аммиака Очищенный от примесей воздух вместе с аммиаком поступает в контактный аппарат. Там происходит каталитическое окисление аммиака.
Ангидриды карбоновых кислот. Кетены. Нитрилы
Ангидриды карбоновых кислот представляют собой продукты отщепления молекулы воды от двух молекул кислоты. Кетены - внутренние ангидриды монокарбоновых кислот. Способы получение и реакции нитрилов. Цианамид представляет собой амид синильной кислоты.
Сахароза свойства и содержание в природе
Text Graphics Сахароза Graphics Сахароза C12H22O11, или свекловичный сахар, тростниковый сахар, в быту просто сахар — дисахарид, состоящий из двух моносахаридов — ?-глюкозы и ?-фруктозы. Сахароза C12H22O11, или свекловичный сахар, тростниковый сахар, в быту просто сахар — дисахарид, состоящий из двух моносахаридов — ?-глюкозы и ?-фруктозы.
Азотная кислота основные понятия
Text Text Graphics Азотная кислота HNO3 Презентация Ученицы 9 класса «б» Гончаренко Инны Graphics Применение Graphics - Это вещество было описано арабским химиком в VIII веке Джабиром ибн Хайяном (Гебер) в его труде «Ямщик мудрости», а с ХV века это вещество добывалось для производственных целей. - Благодаря этому веществу русский учёный В.Ф.
Гидролиз
Гидролизом называется обменная реакция вещества с водой, в результате которой образуются малорастворимые или малодиссоциированные соединения (основания, кислоты, основные соли). Вода является амфотерным электролитом, т. е. она может взаимодействовать и как кислота, и как основание. В первом случае связываются водородные ионы, во втором – гидроксильные ионы.
Электролиз 3
Электро́лиз — физико-химический процесс, состоящий в выделении на электродах составных частей растворённых веществ или других веществ, являющихся результатом вторичных реакций на электродах, которое возникает при прохождении электрического тока через раствор либо расплав электролита.
Промышленное получение азотной кислоты
Варнавский 9в Промышленное получение азотной кислоты. Окисление аммиака Очищенный от примесей воздух вместе с аммиаком поступает в контактный аппарат. Там происходит каталитическое окисление аммиака.
Степень диссоциации
Электролит Формула Степень диссоциации Кислоты Соляная Бромоводородная Йодоводородная Азотная Серная Сернистая Фосфорная Фтороводородная Уксусная
Химия супер-таблица
Растворимость солей, кислот и оснований в воде Ионы – растворяется (>1г на 100г – не растворяется ( – в водной среде разлагается
Производство серной кислоты нитрозным способом
Технологическая схема производства серной кислоты контактным путём хорошо известна из школьных учебников. В нашей стране используется и другой, так называемый нитрозный, способ её получения.
Получение серной кислоты из железного колчедана
Концентрированная серная кислота является сильным окислителем. Проведение окислительно-восстановительных реакций с участием H2SO4 обычно требует нагревания, часто продуктом восстановления является SO2
Желчные кислоты
Реферат по органической химии на тему «Желчные кислоты» Ст.гр. 3-ХДК-84 Зельниченко Анны Александровны г.Днепропетровск 2010г. ЖЕЛЧНЫЕ КИСЛОТЫ, монокарбоновые гидроксикислоты, относящиеся к классу стероидов. Почти все желчные кислоты - производные прир. холановой к-ты (ф-ла Iа).
Характеристики ионоселективных электродов
Марка Диапазон концентраций pX Мешающие ионы Отзывы ЭМ-Ca-01 0.65-4 Mg - 0.2, Ba - 0.02 Na ,K- 0.002, NH4 - 0.003 4.5-10 Теоретический наклон у градуировки бывает редко.
Аланин
Аланин является важным источником энергии для мышечных тканей, головного мозга и центральной нервной системы; укрепляет иммунную систему путем выработки антител; активно участвует в метаболизме сахаров и органических кислот.
Аспаргиновая кислота и глицин
Биологическое действие аспарагиновой кислоты: иммуномодулирующее, повышающее физическую выносливость, нормализующее баланс возбуждения и торможения в ЦНС.
Глютаминовая кислота
Глутаминовая кислота является нейромедиатором, передающим импульсы в центральной нервной системе. Эта аминокислота играет важную роль в углеводном обмене и способствует проникновению кальция через гематоэнцефалический барьер.
Азотная кислота
Структура азотной кислоты. Дымящая азотная кислота. Строение кислоты с МВС.
Живая система
Живая система в условиях Земли - это открытая система состоящая из органических в-в и их компонентов, основными из которых являются белки и нукл. кислоты, обладающая единым метоболизмом, который обеспечивает её саморегуляцию и самовоспроизведение.
Нуклеиновые кислоты
Это высокомолекулярные биополимеры. Впервые были обнаружены в ядре в конце 19в., хотя они есть и в цитоплазме. Они состоят из мономеров, сложных химических соединений, - нуклеотид.
Водородный показатель... Человека
Известно, что кровь здорового человека имеет рН 7,3-7,4. Точнее, плазма крови имеет рН около 7,36 - то есть концентрация катионов оксония H3O+ здесь составляет 4,4 . 10-8 моль/л.
Серная кислота
Технология серной кислоты. Сырье для серной кислоты и методы ее получения.
Абсорбция триоксида серы
Последняя стадия производства серной кислоты. Уравнения химических реакций. Использование в качестве поглотителя менее концентрированной серной кислоты.
Казеин
Казеин, главный белок молока всех млекопитающих. Присутствует в молоке не в свободном виде, а в соединении с кальцием, т.е. как казеинат кальция.
![]() 2,359 мПа*с (15°С);
2,359 мПа*с (15°С);![]() Hoобр
- 548,9 кДж/моль,
Hoобр
- 548,9 кДж/моль,![]() -2853,4 кДж/моль; К 1,147*10-5 (20°С); р-римость в воде 4,97% (25 °С). Образует
бинарные азеотропные смеси с многими в-вами, напр. с бромбензолом (3,5% В.к.;
т. кип. 155,6°С). Соли и эфиры В. к. наз. валератами. Содержится в продуктах
перегонки древесины, бурого угля и др. В пром-сти получают гидроформилированием
1-бутена с послед. окислением образующегося альдегида; окислением амилового
спирта. Наряду с бутилвалератом получается при обработке бутанола СО в присут.
NiI2 и Nal или никеля Ренея в водном р-ре при 340 °С и 37,5 МПа. Эфиры В. к.,
обладающие фруктовым и цветочным запахом (напр., изомилвалерат), -
ароматизирующие в-ва для пищ. продуктов, душистые в-ва в парфюмерии; используют
также как р-рители, сырье в произ-ве лек. в-в.
-2853,4 кДж/моль; К 1,147*10-5 (20°С); р-римость в воде 4,97% (25 °С). Образует
бинарные азеотропные смеси с многими в-вами, напр. с бромбензолом (3,5% В.к.;
т. кип. 155,6°С). Соли и эфиры В. к. наз. валератами. Содержится в продуктах
перегонки древесины, бурого угля и др. В пром-сти получают гидроформилированием
1-бутена с послед. окислением образующегося альдегида; окислением амилового
спирта. Наряду с бутилвалератом получается при обработке бутанола СО в присут.
NiI2 и Nal или никеля Ренея в водном р-ре при 340 °С и 37,5 МПа. Эфиры В. к.,
обладающие фруктовым и цветочным запахом (напр., изомилвалерат), -
ароматизирующие в-ва для пищ. продуктов, душистые в-ва в парфюмерии; используют
также как р-рители, сырье в произ-ве лек. в-в. ![]() 2,731
МПа*с (15°С);
2,731
МПа*с (15°С);![]() 0,024
Н/м (30 °С);
0,024
Н/м (30 °С);![]() 3,03*10-30 Кл*м;
3,03*10-30 Кл*м;![]() -561,5 кДж/моль,
-561,5 кДж/моль,![]() - 2840,8 кДж/моль; К 1,216*10-5 (60°С); раств. в воде (4,2 г в 100 мл),
этаноле, эфире, хлороформе. Соли и эфиры И.к. наз. изовалератами, напр.
этилизовалерат (т. пл. 134,1°С; d420 0,8656, nD20 1,3692; р-римость в воде
0,17%; содержится в ананасах), изоамилизовалерат (жидкость; т. кип. 73-76°С/14
мм рт. ст.; d420 0,8812, nD20 1,4108; в воде раств. плохо).
- 2840,8 кДж/моль; К 1,216*10-5 (60°С); раств. в воде (4,2 г в 100 мл),
этаноле, эфире, хлороформе. Соли и эфиры И.к. наз. изовалератами, напр.
этилизовалерат (т. пл. 134,1°С; d420 0,8656, nD20 1,3692; р-римость в воде
0,17%; содержится в ананасах), изоамилизовалерат (жидкость; т. кип. 73-76°С/14
мм рт. ст.; d420 0,8812, nD20 1,4108; в воде раств. плохо). ![]() метилмасляная)
к-та СН3СН2СН(СН3)СООН (М.к.) - бесцв. жидкость, оптически активна.
(+)-Изомер-т. кип. 86,5-87,5°С/26 мм рт. ст.;d425 0,9313, nD20 1,4058;
метилмасляная)
к-та СН3СН2СН(СН3)СООН (М.к.) - бесцв. жидкость, оптически активна.
(+)-Изомер-т. кип. 86,5-87,5°С/26 мм рт. ст.;d425 0,9313, nD20 1,4058;![]() + 35,56° (неразбавленная к-та). Получают (+ ) - M. к. расщеплением рацемата с
помощью цинхонидина. Содержится в эфирных маслах, напр. лавандовом. (-)-Изомер
- т. кип. 71-72°С/12 мм рт. ст., 64°С/2мм рт. ст; d425 0,9340, nD25 1,4038;
+ 35,56° (неразбавленная к-та). Получают (+ ) - M. к. расщеплением рацемата с
помощью цинхонидина. Содержится в эфирных маслах, напр. лавандовом. (-)-Изомер
- т. кип. 71-72°С/12 мм рт. ст., 64°С/2мм рт. ст; d425 0,9340, nD25 1,4038;![]() —24° (водный р-р; концентрация 0,9 мг/л). Синтезируют (—) - М. к. окислением
2-метил-1-бутанола действием КМnО4 в водно-щелочном р-ре или К2Сr2О7 в среде
H2SO4. При окислении (— )-изомера М. к. действием КМnО4 в водно-щелочном р-ре
получается 2-ги-дрокси-2-метилмасляная к-та. Рацемат М. к.-т. пл. — 48 оС, т.
кип. 176,5°С, 88°С/20мм рт. ст.; d420 0,9361, nD20 1,4060;
—24° (водный р-р; концентрация 0,9 мг/л). Синтезируют (—) - М. к. окислением
2-метил-1-бутанола действием КМnО4 в водно-щелочном р-ре или К2Сr2О7 в среде
H2SO4. При окислении (— )-изомера М. к. действием КМnО4 в водно-щелочном р-ре
получается 2-ги-дрокси-2-метилмасляная к-та. Рацемат М. к.-т. пл. — 48 оС, т.
кип. 176,5°С, 88°С/20мм рт. ст.; d420 0,9361, nD20 1,4060;![]() -557,3 кДж/моль,
-557,3 кДж/моль,![]() -2845
кДж/моль. Синтезируют декарбоксилированием метилэтилмалоновой к-ты,
карбонилированием втор-бутанола действием Ni(CO)4 в присут. NiCl2 и соляной
к-ты при 300 °С и 4 МПа или пропусканием смеси втор-бутанола и СО над NiI2 на
силикагеле при 230°С и 21 МПа, а также гидрокарбонилированием 1-бутена в разб.
уксусной к-те в присут. Ni(CO)4 (при этом образуется и валериановая к-та).
Применяется рацемич. М.к. в произ-ве пластификаторов, синтетич. смазок, лек.
в-в, как экстрагент меркаптанов из углеводородов и стабилизатор виниловых
полимеров.
-2845
кДж/моль. Синтезируют декарбоксилированием метилэтилмалоновой к-ты,
карбонилированием втор-бутанола действием Ni(CO)4 в присут. NiCl2 и соляной
к-ты при 300 °С и 4 МПа или пропусканием смеси втор-бутанола и СО над NiI2 на
силикагеле при 230°С и 21 МПа, а также гидрокарбонилированием 1-бутена в разб.
уксусной к-те в присут. Ni(CO)4 (при этом образуется и валериановая к-та).
Применяется рацемич. М.к. в произ-ве пластификаторов, синтетич. смазок, лек.
в-в, как экстрагент меркаптанов из углеводородов и стабилизатор виниловых
полимеров. ![]() - 565,7 кДж/моль,
- 565,7 кДж/моль,![]() - 2836,6 кДж/моль;
- 2836,6 кДж/моль;![]() 5,7*10-30 Кл*м; К 0,732*10-5 (60°С); р-римость в 100 г воды 2,2 г (20°С). Р-ции
П. к. осложнены стерич. препятствиями, связанными с экранированием
карбоксильной группы СН3-группами. Напр., П. к. труднее этерифицируется, чем
другие В.к.; эфиры ее более устойчивы при гидролизе и окислении. При окислении
Н2О2 в присут. FeSO4 в водном р-ре H2SO4 П. к. превращается в
2,2,5,5-тетраметиладипиновую к-ту НООСС(СН3)2СН2СН2С(СН3)2СООН, хлорируется при
облучении УФ-светом (
5,7*10-30 Кл*м; К 0,732*10-5 (60°С); р-римость в 100 г воды 2,2 г (20°С). Р-ции
П. к. осложнены стерич. препятствиями, связанными с экранированием
карбоксильной группы СН3-группами. Напр., П. к. труднее этерифицируется, чем
другие В.к.; эфиры ее более устойчивы при гидролизе и окислении. При окислении
Н2О2 в присут. FeSO4 в водном р-ре H2SO4 П. к. превращается в
2,2,5,5-тетраметиладипиновую к-ту НООСС(СН3)2СН2СН2С(СН3)2СООН, хлорируется при
облучении УФ-светом (![]() =
365,5 нм) в 3-хлор-2,2-диметилпропионовую к-ту С1СН2С(СН3)2СООН, при взаимод. с
РС13, РС15, SOC12 или СОС12 образуется пивалоилхлорид. Соли и эфиры П. к. наз.
пивалатами, напр. этилпивалат (т. пл. 89,5 °С, т. кип. 119°С).
=
365,5 нм) в 3-хлор-2,2-диметилпропионовую к-ту С1СН2С(СН3)2СООН, при взаимод. с
РС13, РС15, SOC12 или СОС12 образуется пивалоилхлорид. Соли и эфиры П. к. наз.
пивалатами, напр. этилпивалат (т. пл. 89,5 °С, т. кип. 119°С). 
