2.6. КРУГООБОРОТЫ ВЕЩЕСТВ В БИОСФЕРЕ
Основой динамического равновесия и стойкости биосферы является кругооборот веществ и превращения энергии, который состоит из многообразных процессов. Хорошо известны глобальные процессы кругооборота воды, кислорода, углерода, азота, фосфора, микроэлементов на Земле. В.Р. Вильямс писал, что единственный способ придать чему-то конечному свойства бесконечного – это заставить конечное вращаться по замкнутой кривой, то есть вовлечь его в кругооборот. В этом высказывании есть доля философского и религиозного понимания сути кругооборотов веществ и превращения энергии. Выделяют два основных кругооборота: большой (геологический) и малый (биологический). Геологический кругооборот веществ имеет наибольшую скорость в горизонтальном направлении между сушей и морем. Смысл большого кругооборота в том, что горные породы подвергаются разрушению, выветриванию, а продукты выветривания, в том числе растворимые в воде питательные вещества, сносятся потоками воды в Мировой океан с образованием морских напластований и возвращаются на сушу лишь частично, например, с осадками или с извлеченными человеком из воды организмами. Далее в течение длительного временного отрезка протекают медленные геотектонические изменения – движение материков, поднятие и опускание морского дна, вулканические извержения и т.д., в результате которых образовавшиеся напластования возвращаются на сушу и процесс начинается вновь. Малый кругооборот, являясь частью большого, происходит на уровне биогеоценоза. Он состоит в том, что питательные вещества почвы, вода, CO2 и другие вещества из атмосферы за счет фотосинтеза аккумулируются в веществе продуцентов (растений и некоторых бактерий), расходуются на построение тел и жизненные (обменные) процессы продуцентов и консументов. Затем в основном за счет редуцентов органические вещества разлагаются и частью минерализуются, вновь становятся доступными растениям и снова ими вовлекаются в поток вещества (кругооборот). Скорость перемещения веществ при биологическом кругообороте значительно выше, чем при геологическом. Кругооборот (перемещение) химических веществ из неорганической среды через растительные и животные организмы обратно в неорганическую среду с использованием солнечной энергии с протеканием биохимических превращений (реакций) носит название биогеохимического цикла. Годичные биогеохимические циклы приводят в движение примерно 480 млрд т веществ, в основном биофильных элементов – углерода, азота, водорода, кислорода и др.
2.6.1. Кругооборот углерода
Э![]() тот
кругооборот,
как и большая
часть других
кругооборотов,
может быть
представлен
в виде упрощенной
схемы (рис. 2.5.):
тот
кругооборот,
как и большая
часть других
кругооборотов,
может быть
представлен
в виде упрощенной
схемы (рис. 2.5.):
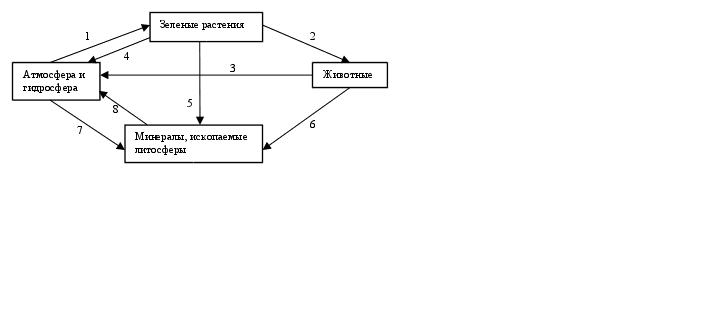
Рис. 2.5. Кругооборот углерода
Кругооборот углерода, как и любого другого элемента, совершается как по большому, так и по малому циклам.
Большой (геологический) кругооборот углерода можно представить в виде схемы (рис. 2. 6.).
В атмосфере и водных источниках присутствует углекислый газ СО2. Под его действием, а также при участии ветра и воды (Н2О) частью изменяется состав горных пород (например, карбонатных: известняка СаСО3, магнезита МgCO3, доломита СаСО3МgCO3):
СаСО3 + СО2 + Н2О Са(НСО3)2
МgCO3 + СО2 + Н2О Мg(НСО3)2 .
Образующиеся растворимые соли (гидрокарбонаты) вымываются и выносятся в океан, частью насыщает воду океана. Частью же под воздействием неорганических условий и фильтрации воды через живые организмы (например, моллюски) эта соль преобразуется и отлагается на дне океана в виде осадочных пород (того же, например, СаСО3, частью представленного в виде ракушечника, как остатки раковин умерших моллюсков) (пункты 6, 7 рис. 2.5.). Осадочные породы претерпевают метаморфоз (различные превращения), а также под действием тектонических сил перемещаются в глубину земной коры, откуда частью через длительный период поднимаются на поверхность, а быстрее идут процессы под действием вулканических извержений, которые являются вновь источниками углерода в атмосфере в виде СО2, а иногда и СО, окисляющегося до СО2.
Биотический кругооборот углерода – составная часть большого кругооборота, он связан с жизнедеятельностью организмов.
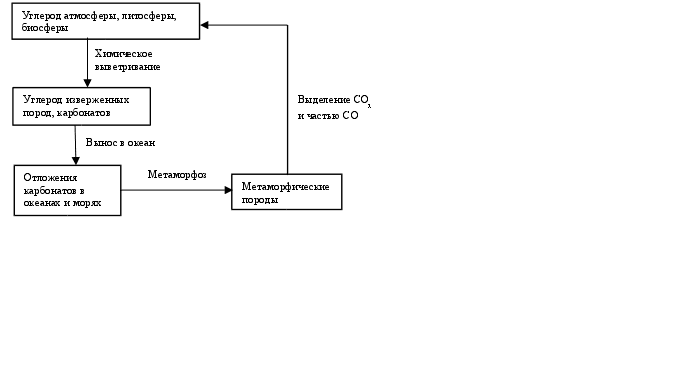
Рис. 2.6. Большой (геологический) кругооборот углерода
Запасы углерода, содержащегося в виде СО2, в атмосфере составляют 23,51011 т. Органическое вещество синтезируется зелеными растениями из СО2 атмосферы (пункт 1, рис. 2.5.), содержание которого там лишь 0,03 – 0,04 % (табл.2.8), а затем вместе с веществом растений (продуцентов) потребляется консументами разных трофических уровней (пункт 2, рис. 2.5.).
Синтез органических веществ зеленые растения осуществляют с помощью энергии солнечного излучения из СО2 и Н2О в процессе фотосинтеза.
Таблица 2.8. Количество углекислого газа в атмосфере и его кругооборот, в кг
| По Ю.Саксу | По Г.Гредеру | По Е.Рейнау | |
|
Количество СО2 |
25001012 |
21001012 |
15301012 |
| Усваивается растениями за год |
6481012 |
601012 |
86,51012 |
|
За сколько лет растения вычерпали бы запасы СО2 в атмосфере |
4 | 35 | 18 |
Значение света для зеленых растений подчеркивал еще Аристотель: «Те части растений, в которых влажное не смешивается с солнечными лучами, остаются белыми».
В 1777 г. Д. Пристли открыл, что растения днем выделяют кислород, очищая воздух, «испорченный» горением или дыханием животных. Сам процесс фотосинтеза был досконально изучен К.А. Тимирязевым (1843-1920). По Тимирязеву, процесс фотосинтеза протекает под воздействием содержащегося в зеленых частях растений сложного органического вещества – хлорофилла, спектр поглощения которого показан на рис. 2.7. Коэффициент использования энергии солнечного света при фотосинтезе невелик ( порядка 2 %).

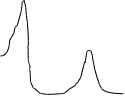 Поглощение
Поглощение
420 500 580 660 740 Длина волны, мкм
Рис. 2.7. Спектр поглощения хлорофилла
Усвоение СО2 растениями при фотосинтезе эндотермический процесс, который протекает с поглощением большого количества теплоты с Н=112 ккал/моль в случае синтеза глюкозы:
h
6СО2 + 6Н2О = С6Н12О6 + 6О2 – 674 ккал.
В 1961 г. за раскрытие механизма фотосинтеза американскому ученому М. Келвину присуждена Нобелевская премия. Механизм фотосинтеза такой: попадая в клетку зеленого листа, СО2 присоединяется к акцептору (углеводрибулезодифосфат), с которым продолжается дальнейшее передвижение и превращение. Благодаря ферменту альдолазы образуется глюкоза С6Н12О6, а далее – сахароза С12Н22О11, крахмал (С6Н10О5)n и другие углеводы Сn(Н2О)m. Суммарно фотосинтез можно выразить так:
h
nСО2 + mН2О = Сn(Н2О)m + nО2 – Q.
Фотосинтез осуществляется за счет энергии солнечных лучей (26500 млрд ккал/с на всей земной поверхности).
Часть синтезированного в этом процессе вещества снова переходит к акцептору. Так и реализуется циклический процесс. Только циклические процессы могут быть саморегулирующимися (фотосинтез в их числе). Дальше с помощью других ферментов из углеводов синтезируются белки, жиры и другие нужные для жизни растений органические вещества.
Следует заметить, что содержание СО2 в атмосфере невелико, и он бы полностью исчерпался за 4-35 лет (табл. 2.8.).
Откуда же он поступает в атмосферу? Ежегодно все растения и животные выдыхают СО2 1013-1014 кг, а люди – 1,081012 кг (пункты 3,4; рис.2.5).
Экзотермическая реакция окисления углерода до СО2 протекает в тканях живого организма под действием вдыхаемого кислорода, который переносится по кровеносной системе посредством гемоглобина – сложного органического вещества (с молярной массой М68000 г/моль), содержащего 4 атома железа, каждый из которых способен связывать одну молекулу О2.
Процесс дыхания упрощенно можно изобразить схематически так (где Гем – гемоглобин):
1) Гем + О2 = ГемО2 (легкие: вдыхание);
2) Перенос с кровью в ткани;
3) ГемО2 + С (из пищи) = ГемСО2 (ткани);
4) Перенос в легкие;
5) ГемСО2 = Гем + СО2(легкие: выдыхание).
Таким образом, можно сказать, что гемоглобин ведет себя как катализатор. Другие источники поступления СО2 в атмосферу – извержения вулканов, кислотные дожди, действующие на известняки (пункт 8, рис. 2.5). Часть СО2 образуется при гниении, разложении, отмирании живых организмов под действием редуцентов, а также при пожарах и, наконец, при антропогенном воздействии. Так, ежегодно в промышленности и на транспорте при сжигании топлива выбрасывается в атмосферу 1,51012 кг СО2 и эта цифра ежегодно растет, что создает глобальную проблему - парниковый эффект.
Если бы не происходило побочных процессов, то количество СО2, выделяемого в атмосферу и усваиваемого растениями, было бы одинаковым. Однако же часть углерода временно выводится из кругооборота за счет частичной минерализации останков растений (пункт 5, рис. 2.5) и животных (пункт 6, рис. 2.5) с образованием торфа, нефти, углей и других ископаемых в литосфере.
Общее количество углерода земной коры (трех оболочек), по Вернадскому, составляет примерно 11017 т, причем большая часть его рассеяна повсюду в природе, поэтому такой разброс в данных по распределению его по отдельным формам нахождения (табл. 2.9).
Таким образом, основная масса углерода принимает участие в медленном геологическом кругообороте. Естественно предположить, что в настоящее время атмосфера содержит лишь ничтожную часть СО2 от того запаса, который первоначально имелся, и углерод постепенно выводился из биологического кругооборота из-за отложений в литосфере. Но из-за антропогенных факторов (использование горючего, его сгорания) в последнее время доля СО2, а значит, и углерода в атмосфере неуклонно растет из года в год.
Таблица 2.9. Количество углерода, в т
Скопление углерода |
Количество углерода, т | |
| По Вернадскому | По Г.В. Стадницкому и А.И. Родионову | |
| Атмосфера |
31012 |
2,351012 |
| Океан |
11014 |
- |
| Карбонатные отложения | - |
1,31016 |
| Кристаллические породы | - |
11016 |
| Известняки |
31016 |
- |
| Живое вещество |
11012 |
51011 |
| В растительных тканях | - |
51011 |
| В животных тканях | - |
5109 |
| Каменные угли |
21013 |
- |
| В каменных углях + нефти | - |
3,41015 |
Большим регулятором содержания СО2 в атмосфере является Мировой океан. Много углерода исключается из биологического кругооборота веществ на суше и попадает в океан в основном в виде карбонатных солей. Если в атмосфере повышается содержание СО2, то часть его растворяется в воде, вступает в реакцию с СаСО3, с образованием растворимых в воде гидрокарбонатов, например Са(НСО3)2. Наоборот, при уменьшении содержания СО2 в атмосфере, гидрокарбонаты, которые всегда содержатся в морской воде, превращаются в карбонаты, которые выпадают из раствора, частью используются организмами для построения скелетов или панцирей (раковин) животных, при отмирании, а частью и без отмирания в виде СаСО3 оседают на морское дно. Таким образом, существует обратимый процесс:
уменьшение концентрации СО2
Са(НСО3)2 СаСО3 + Н2О + СО2 .
увеличение концентрации СО2
2.6.2. Кругооборот кислорода
Один из наиболее сложных кругооборотов, так как с кислородом О2 вступает в реакцию большое количество органических и неорганических веществ, а также водород (последний дает с О2 воду Н2О). Упрощенная схема кругооборота кислорода представлена на рис. 2.8).
Кругооборот кислорода непосредственно связан с кругооборотом углерода (процессы фотосинтеза, дыхания и питания животных). Особенностью кругооборота кислорода является широкое многообразие кислородсодержащих веществ в биосфере. Кислород в
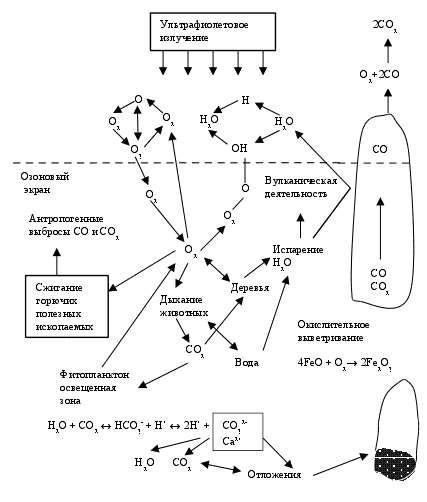
Рис. 2.8. Кругооборот кислорода
целом самый распространенный в биосфере химический элемент. В свободном виде (О2) он присутствует в наземных водных источниках, в почве и составляет основу воздуха, присутствуя в атмосфере также и в виде озона (главным образом в стратосфере). Роль озона в биосфере, его образование подробно рассматривается в других разделах пособия. В связанном виде кислород составляет основу горных пород и минералов (например, солевых и оксидных), а также газообразных продуктов (например, оксидов углерода, серы, азота и др.), и, наконец, воды (самого распространенного на планете вещества), образование которых рассматривается в других кругооборотах элементов и веществ.
Нарушение стабильного кругооборота кислорода происходит в основном из-за больших объемов сжигания органического топлива (свободный кислород тратиться на окисление), а с другой стороны, из-за массовой вырубки лесов (главного источника поступления свободного кислорода в биосферу). Одновременно с этим возникает целый блок глобальных проблем (парниковый эффект, кислотные дожди, явления "смога" и др.).
2.6.3. Кругооборот серы
Существуют гипотезы, что в ранние геологические эпохи Земли недостаток О2 предполагал существование серы в основном в виде Н2S и солей (главным образом, сульфидов, например FeS2). С формированием О2 начинаются окислительные процессы. В наше время сера на планете присутствует в виде Н2SО4 и Н2S (и их солей), и части свободной серы, SО2 , а также в виде органических веществ в живых организмах.
Величайшую роль в кругообороте выполняют бактерии. Мы уже знакомы с фотосинтезом, но, кроме этого, некоторые бактерии, используя энергию химических экзотермических реакций окисления (хемосинтез), синтезируют органические вещества. Так под действием особого вида бактерий (серобактерии) идет окисление Н2S до S:
2Н2S + О2 2Н2О + 2S + 127 ккал (+ Q).
Cера откладывается в «телах» серобактерий, составляя до 95 % их общей массы, тем самым устраняя вредное действие Н2S на растения и животных. Это неполный процесс окисления серы, он идет и дальше до Н2SО4 под действием О2 воздуха, а также пурпурных бактерий, для которых дыхание заменяется процессом:
бактерии
Н2S + 2О2 Н2SО4 + 189 ккал.
Сера окисляется на воздухе, а также в организмах серобактерий, если они будут лишены сероводородной среды:
2S + 3О2 + 2Н2О = 2Н2SО4 + 251 ккал,
SО2 или Н2SО3 – практически не образуются, а образуется Н2SО4, так как протекают достаточно сложные процессы:
2S + 2О2 + 2Н2О = 2Н2SО3 + 157 ккал, (1)
2Н2SО3 + Н2О + O2 = 2Н2SО4 + 94 ккал. (2)
Вторая реакция протекает быстрее, поэтому Н2SО3 (или же SО2 + Н2О) не накапливается. Свободная Н2SО4 в природе встречается редко (разве что при кислотных дождях), она очень активна, поэтому реагирует с содержащимися в почве и воде веществами или горными породами, например:
СаСО3 + Н2SО4 = СаSО4 + СО2 + 2Н2О.
Большая часть сульфатов уносится водами рек, а также под действием осадков и выветривания минералов, в моря, частью растворяясь в океанических водах, а частью откладываясь на дне в виде напластований и образуя минералы, особенно природного гипса СаSО42Н2О, перемещаясь в глубины литосферы, а затем через годы – на поверхность и т.д.
Попадая в глубокие слои литосферы, тот же СаSО4, претерпевает восстановительный процесс, например, с участием органических веществ:
СаSО4 + СН4 СаS + СО2 + 2Н2О СаСО3 + Н2S + Н2О.
Таким образом, возникают сероводородные («серные») источники (например, Мацеста, Пятигорск). Но существуют и другие бактерии – сульфатовосстанавливающие, которые питаются за счет сульфатов. Так, на глубине ниже 150 м, например, в Черном море, сульфаты под действием этих бактерий восстанавливаются до сероводорода, который, поднимаясь наверх, вновь подвергается действию серобактерий, окисляется до SО42-, а часть Н2S уходит в атмосферу. Источники Н2S – болота, вулканическая деятельность, природные процессы гниения отмерших живых организмов.
При извержении вулканов выделяется Н2S и SО2, концентрации которых могут быть различными, тогда возможно протекание реакции: 2Н2S + SО2 3S + 2Н2О.
При избытке Н2S, выделяющаяся сера защищается от окисления и потому может образовывать на некоторой глубине в толще литосферы – пласты S или вкрапления.
Кроме того, на больших глубинах формируются горючие природные ископаемые (тот же уголь, и углеводороды, содержащие серу), откладываются сланцы и другие осадочные породы, содержащие серу.
При добыче этих ископаемых, их сжигании или химической переработке, а также их естественном разложении в атмосферу выбрасываются SО2 и Н2S, которые окисляются до Н2SО4 и, наряду с природными источниками, затем выпадают на землю в виде осадков – кислотных дождей. И так, круг замыкается. Особенно из-за деятельности человека, а также из-за окислительной способности воздуха в наше время кругооборот осуществляется с увеличением содержания сульфатов, а в прошлом – преобладали сульфиды.
Остался неучтенным процесс потребления серы растениями, с учетом которого кругооборот серы можно выразить упрощенной схемой (рис. 2.9).
Переработка сульфатов растениями, в том числе и с использованием бактерий, очень сложный процесс, приводящий к синтезу растениями серосодержащих белковых веществ.
Животные, питающиеся растениями, также путем биохимических процессов синтезируют серосодержащие вещества, характерные для своих организмов. При отмирании животных и растений, их белковые вещества разлагаются до Н2S и некоторых других серосодержащих продуктов, и кругооборот серы продолжается.

Рис. 2.9. Кругооборот серы (упрощенно)
Кругооборот серы можно представить схемой (рис. 2.10).

H2SO4
Рис. 2.10. Кругооборот серы
2.6.4. Кругооборот азота
Азот составляет примерно 78 % воздуха атмосферы. Часть его содержится в почве и в воде в виде неорганических соединений (в виде аммонийных солей, а также нитритов и нитратов), а часть – в форме органических соединений, входящих в состав растительных и животных белков, аминокислот. Существует большой кругооборот азота, включающий сушу и атмосферу, частью которого является малый кругооборот (биотический). Общая упрощенная схема кругооборота азота представлена на рис. 2.11.
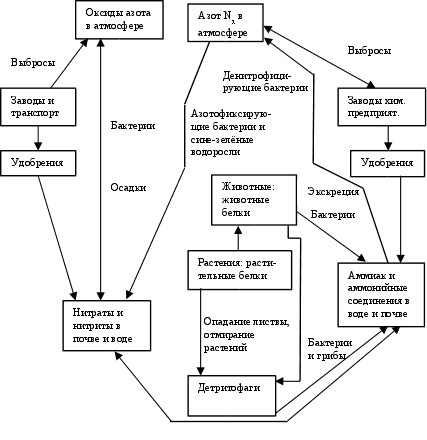
Бактерии
Рис. 2.11. Кругооборот азота (упрощенно)
Биогеохимический цикл азота с учетом антропогенных факторов рассмотрим подробнее. Азот в свободном виде (в виде N2) недоступен растениям. Для своего роста растения могут использовать лишь соли азотной и азотистой кислот, хуже – аммиачные соединения.
На границе воздушной атмосферы и грунта содержится от 0,02 до 0,056 кг/м3 азота (летом и осенью больше, чем зимой и весной, из-за грозовых разрядов). За год на 1 га в разных частях земли выпадает 2,6-14,3 кг азота. Больше всего азота вблизи больших химических предприятий, связанных с продуктами азота, поэтому в почву в радиусе нескольких километров азотных удобрений не следует вносить.
Как же азот из воздуха попадает в почву в связанном виде? Это возможно благодаря азотофиксирующим бактериям, живущим в грунтах, а также сине-зеленым водорослям в водоемах. Поэтому их значение необычайно велико. Примерами таких бактерий являются аэробные азотобактерии (действуют в присутствии кислорода воздуха), анаэробные клостридиумы Пастера (действуют без доступа О2), клубеньковые бактерии, живущие и функционирующие в корнях-клубнях, в основном бобовых растений. Процесс фиксации таков:
N2 + 3Н2 2NН3 + 615,63 кДж.
(или 2N)
За год эти бактерии могут запасать для растений до 20 –30 кг азота. Затем начинают выполнять свои функции нитрифицирующие бактерии (упрощенно - нитритные и нитратные), окисляющие аммиак (соответственно, до азотистой и азотной кислот):
2NН3 + 3О2 2НNО2 + 2Н2О + 148 ккал;
2НNО2 + О2 2НNО3 + 48 ккал.
Эти кислоты в процессе обменных реакций в грунтовых растворах образуют соли (нитриты и нитраты), которыми питаются растения:
К2СО3 + 2НNО3 2КNО3 + СО2 + Н2О.
(или СаСО3)
Растения используют нитраты для синтеза белковых соединений, которые идут для питания другим живым организмам (например, животным), синтезирующим свои аминокислоты и т.д. Продукты выделения (экскреция) – мочевина и другие, трупы растений и животных подвергаются деструкции и минерализуются сначала до аммиака и аммиачных соединений (аммонификация) под действием бактерий, грибов, дождевых червей и др., и далее до солей азотных кислот, а последние денитрифицирующими бактериями до N2, уходящего в атмосферу (реакция 1). Частью в атмосферу азот удаляется и в виде NН3. Затем начинается новый цикл.
5С6Н12О6 + 24КNО3 30СО2 + 18Н2О + 24КОН + 12N2 + 9388,3 (1)
кДж/моль.
Часть аммиака после аммонификации в почве нитрифицируется бактериями до солей (нитритов и нитратов) и остается в почве для питания растений.
Итак, существуют азотофиксирующие бактерии (азот переводят в NН3), нитрифицирующие (аммиак - в основном, в соли НNО3), а денитрифицирующие разлагают нитратные соли, превращая их в NН3 и даже до N2. Поэтому первые и вторые бактерии обогащают грунт доступными для растений формами азота, а третьи – обедняют грунт азотом.
Более полная схема кругооборота азота представлена на рис.2.12.

Рис. 2.12. Схема биотического кругооборота азота по Р.Риклефсу (1979 г.)
В геологический кругооборот постоянно поступает часть азота в виде различных соединений, частью используемых в сельском хозяйстве в качестве азотных удобрений. Азотсодержащие вещества частью поступают и в реки, благодаря стоку которых выносятся в моря. Часть азота попадает в реки и далее в моря за счет осадков, например, кислотных дождей (содержащих НNО3), из-за выбросов оксидов азота (а также образования оксида азота в атмосфере при грозах). Наибольшее содержание соединений азота в районах впадения рек в моря, наименьшее – в центральных частях океанов. Азотсодержащие соединения используются водорослями для синтеза органических веществ и поступают в кругооборот океана, часть постепенно оседает на дно, потому, вынесение азота с суши не увеличивает его концентрацию в морской воде. Неуправляемая же деятельность людей может привести к сильному загрязнению окружающей среды, что нарушит природный баланс. Тревожные изменения в биосфере уже и сейчас столь заметны. Это цветение рек, чрезмерное размножение сине-зеленых водорослей, ускоряющееся заболачивание природных водоемов, ухудшение качества воды и т.д.
2.6.5. Кругооборот фосфора
Кругооборот фосфора достаточно сложен. Рассмотрим его в упрощенном виде. Фосфор один из наиболее важных биогенных элементов, так как входит в состав нуклеиновых кислот, костной ткани, клеточных мембран, систем переноса энергии (АТФ) и др. Кругооборот фосфора также совершается по большому и малому циклам, но всецело связан с жизнедеятельностью организмов. Фосфор – подвижный элемент, поэтому его кругооборот зависит от множества факторов окружающей среды, а в наше время особенно - от антропогенных. Так, фосфор активно поступает в водные источники в виде моющих средств (детергентов), фосфорных и комбинированных удобрений с полей, отходов промышленности (особенно продуктов переработки фосфорсодержащих минералов – апатитов и фосфоритов) и др. Это приводит к нарушению равновесия в биогенном кругообороте фосфора, представленного на рис. 2.13.
Усвоение фосфора растениями в значительной степени зависит от кислотности почвенного раствора. Так, в воде (в среде близкой к нейтральной) фосфаты натрия, калия, кальция и других металлов слаборастворимы, в щелочной среде (при рН 7) – практически нерастворимы, а с повышением кислотности постепенно превращаются (рис.2.14) в хорошо растворимые - фосфорную кислоту Н3РО4 и NаН2РО4, относительно растворимую соль Са(Н2РО4)2, которые хорошо усваиваются растениями.
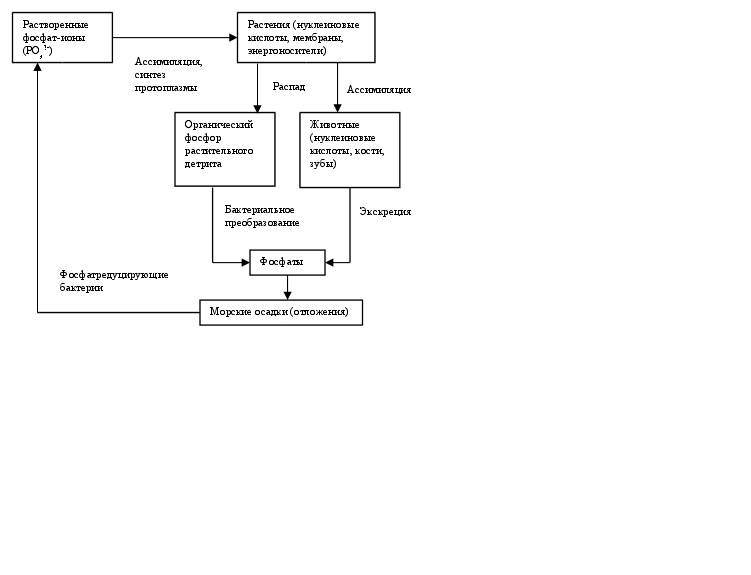
Рис. 2.13. Схема биотического кругооборота фосфора по Р.Риклефсу (1979 г.)
По распространенности в биосфере фосфор не рекордсмен, но многие организмы выработали различные приспособления для улавливания и накопления этого элемента в концентрациях, значительно превышающих его содержание в окружающей среде (особенно в воде).
Увеличение кислотности с уменьшением рН среды
Ионная форма: РО43- НРО42- Н2РО4- Н3РО4
соль: Na3РО4 Na2НРО4 NaН2РО4 очень
растворимость: слегка (средняя) средняя хорошо хорошо
растворимость растворимость растворима растворима
соль: Ca3(РО4)2 CaНРО4 Ca(Н2РО4)2
растворимость: нерастворима нерастворима малорастворима
Рис. 2.14. Растворимость фосфора по Р.Риклефсу (1979 г.)
Так, вдоль юго-восточного побережья Америки обитают моллюски (небольшая колония) – биомассой 12 кг на 1 м2. Эти моллюски относятся к типу фильтрантов. Они фильтруют воду, извлекая из нее мелкие организмы и детрит, богатый фосфором и другими элементами в мелководной зоне прилива. Расчет показал, что кругооборот частиц, содержащих фосфор, в этой зоне происходит всего за 2,6 суток. За это время моллюски извлекали фосфор в количествах, соответствующих его среднему содержанию во всех взвешенных частицах. Этот моллюск, являясь второстепенным компонентом прибрежного сообщества (малая пищевая ценность для других живых существ), оказывает громадное значение на кругооборот и удержание ценного фосфора.
Фосфор накапливается в виде соединений на дне океана на небольших глубинах, откуда из-за геологических изменений оказывается в литосфере, а со временем и в верхних слоях литосферы (например, в виде апатитов и фосфоритов). Существуют апатиты и вулканического происхождения.
Часть отложений соединений фосфора остается в осадке в неглубоких водах и включается в повторный кругооборот, посредством диатомей (вид водорослей), которые накапливают фосфор. Отмирая, они являются источниками фосфора.
Кругооборот воды в биосфере будет рассмотрен в разделе "Атмосфера".
3.2. ЛИТОСФЕРА ЗЕМЛИ
Литосфера - верхняя твердая оболочка Земли, включающая земную кору и часть верхней мантии (толщина литосферы 50-100 км, хотя некоторые авторы говорят и мощности свыше 100 км).
Земная кора имеет также слоистое строение:
верхний слой с низкими параметрами температуры и давления - кора выветривания (осадочный слой, содержащий осадочные породы - например, песок, глину, известковые образования и др.) мощностью на суше 0,5-0,8 км, включает и дно гидросферы (например, ил толщиной 1-1,5 км). Самый тонкий (в среднем 1-1,5 м) поверхностный слой и важнейший в биосфере - почва.
гранитовый слой (более плотный), который на дне океана сильно истончается и даже может отсутствовать;
базальтовый слой (еще с большей плотностью).
Химический состав земной коры определяется содержанием в ней, прежде всего, 8 наиболее распространенных элементов (в массовых %, по Вернадскому и Ферсману): кислород (О)- 49,5, кремний (Si) - около 26, алюминий (Al) - 7,4, железо (Fe) - 4, кальций (Са) - 3, натрий (Na) - 2,6, калий (К) - 2,4, магний (Mg) - 1,9. Важнейшим составляющим литосферы и гидросферы является почва.
3.2.1. Почва
3.2.1.1. Общая характеристика почв
Почва - самый верхний тончайший слой суши, образовавшийся под влиянием живых организмов, климатических процессов (выветривания - воздействия ветра и осадков, колебания температур и др.), сейсмических и механических процессов из материнских (земных) горных пород.
Плодородная почва - важнейший для человека ресурс, так как это залог производства почти всех продуктов питания. 95 % продовольствия человек получает от земель и только 5 % из океана. Обилие земельных и водных ресурсов - главное условие процветания цивилизации.
Толщина почвенного покрова невелика (например, толщина наиболее плодородных почвенных образований - черноземов на равнинах в среднем 1-1,5 м), хотя с увеличением высоты (по отношению к уровню моря) почвенный покров истончается, а порой и отсутствует, и тем самым материнская порода выходит на земную поверхность. Современный состав почвенного покрова Земли: 28 % приходится на леса, 17 % - луга, 10 % - пашни, 45 % - остальную сушу. Структура почвы - это совокупность агрегатов (комочков почвы), обладающих различной величиной, формой и определенными физико-химическими свойствами. Так, высокоплодородные тучные глинистые черноземы имеют хорошо выраженную водопрочную комковато-зернистую структуру. Упрощенная схема строения почвы может быть выражена следующим образом (рис. 3.1.):
_____________________________________________
самый тонкий слой - подстилка
---------------------------------------------------------------------
слой перегноя
______________________________________________
слой вымывания
______________________________________________
слой накопления минеральных солей
______________________________________________
подпочва
______________________________________________
Рис. 3.1. Упрощенная схема строения почвы
Собственно к почве обычно относят средние три слоя. Чем больше слоев (более мощный горизонт), тем выше обычно плодородие почвы. Почва (по Вернадскому) - это биокосное вещество. Главные компоненты почвы:
минеральные частицы (песок, глина и др.), состоящие, главным образом, из 8 вышеприведенных наиболее распространенных в земной коре химических элементов);
детрит - отмершее органическое вещество (остатки от растений, животных и микроорганизмов);
множество живых организмов (от растений и животных до детритофагов и редуцентов). Это насекомые, грибы, бактерии, дождевые и другие виды червей, простейшие и др.
Роль большинства этих живых организмов состоит в переводе детрита в гумус (органические вещества во многом определяющие плодородие почвы). Так, в тучных черноземах имеется гумусовый горизонт толщиной 60-70 см, а содержание гумуса может достигать 15 %. Плотность такой почвы, благодаря органическому гумусу, составляет 1,1-1,2 г/см3, в отличие от песчаных почв плотностью свыше 2 г/см3 при малом содержании гумуса. Средний же состав почвы: 93 % минеральных и 7 % органических веществ. Площадь черноземов на нашей планете сейчас составляет примерно 600 млн га. Большая часть их представлена на равнинах. Ведущим специалистом в мире в области почвоведения был русский профессор В.В. Докучаев. Он же подробно изучил черноземы России. Лучшими по показателям были признаны тучные карловские черноземы - Полтавской губернии и воронежские. В качестве идеального образца и сейчас во Франции в метрологическом музее пребывает образец чернозема именно Воронежской губернии. Основные типы почв на территории России это: черноземы, подзолистые, дерново-подзолистые, подзолисто-болотные, серые лесостепные, пойменные, солончаки и др.
3.2.1.2. Свойства почвы как среды обитания
Свойства различных типов почв определяют эдафогенные факторы, которые ниже и рассматриваются.
3.2.1.2.1. Минеральные элементы питания и способность
почвы их удерживать
Для питания растений необходимы такие минеральные, питательные компоненты (иными словами биогены), как нитраты (NO3-), фосфаты (PO43-), калий (K+) и кальций (Ca2+). За исключением соединений азота, которые образуются из атмосферного N2 в процессе круговорота, все биогены изначально входят в химический состав горных пород наряду с “непитательными” элементами, такими как кремний и алюминий. Однако эти биогены недоступны растениям, пока они закреплены в структуре пород. Чтобы ионы биогенов перешли в менее связанное состояние или в водный раствор, порода должна быть разрушена.
Порода, которую называют материнской, разрушается в процессе естественного выветривания.
Выветривание включает процессы:
воздействие ветра и воды
замерзание и оттаивание;
нагревание и охлаждение;
абразивное действие песчаных частиц;
биологические факторы (растения в мелких трещинах и др.);
химическое воздействие.
Когда ионы биогенов высвобождаются, они становятся доступными для питания растениям, но могут также вымываться просачивающейся сквозь почву водой. Последний процесс называется выщелачиванием.
Выщелачивание почв - вымывание из почвы или отдельного ее горизонта растворимых веществ под влиянием нисходящего или бокового тока почвенного раствора. Эти вещества могут выноситься за пределы почвы или накапливаться в одном из ее горизонтов (расположенный параллельно поверхности относительно однородный слой почвы, обособившийся в процессе почвообразования).
Выщелачивание не только снижает плодородие почв, но и способствует загрязнению среды. Способность почвы связывать и удерживать ионы биогенов, чтобы они не выщелачивались и могли поглощаться корнями, называют ионообменной емкостью почвы.
Будучи исходным источником биогенов, выветривание все же слишком медленный процесс, чтобы обеспечить нормальное развитие растений. В естественных системах основной источник биогенов - разлагающиеся детрит и метаболические отходы животных, то есть кругооборот биогенов. Если ионообменная емкость утрачена, то биогены выщелачиваются и плодородие падает.
В агроэкосистемах происходит неизбежное удаление биогенов с собранным урожаем, так как они входят в состав растительного материала. Поэтому их запас постоянно пополняют, внося удобрения:
неорганические (химические) смесь минеральных биогенов (нитраты, фосфаты, калийные удобрения и др.);
органические (растительные остатки и отходы, например, навоз).
Даже при внесении удобрений ионообменная емкость почвы сохраняет свое жизненно важное значение.
Выщелачивание удобрений наносит экономический ущерб и загрязнение водоемов, а порой приводит к эвтрофикации водоемов, сопровождающейся массовым размножением сине-зеленых водорослей, уменьшением концентрации свободного кислорода в воде и массовой гибелью многих обитателей водоемов, а особенно рыб, изменением видового состава бактерий и т.д.
3.2.1.2.2. Вода и водоудерживающая способность почвы
В листьях растений существуют тонкие поры, через которые происходит поглощение углекислого газа (CO2) и выделение кислорода (O2) в процессе фотосинтеза. Однако они же пропускают пары воды из клеток растения с поверхности листьев в атмосферу. Это явление транспирации, на которую расходуется 99 % всей поглощаемой растениями воды, на фотосинтез же расходуется менее 1 % . Недостаток воды определенно сказывается на росте и развитии растений. Очевидно, что если вода стекает с поверхности, а не впитывается, пользы от этого не будет. Поэтому важна инфильтрация (способность воды просачиваться в глубь почвы и далее). Причем вода, просачивающаяся в нижние слои (ниже 1 – 1,5 м), для многих растений становится недоступной. Для растений важна вода, удерживаемая слоем почвы. Величина этого запаса воды называется водоудерживающей способностью почвы. Даже при редких осадках почвы с хорошей водоудерживающей способностью могут запасти достаточно влаги для поддержания жизни растений.
Кроме этого, запас воды в почве сокращается не только в результате его использования растениями, но и за счет испарения с поверхности почвы. Чтобы его уменьшить, создают растительный покров.
Таким образом, идеальной может считаться такая почва, которая имеет следующие характеристики:
1) инфильтрация - хорошая;
2) водоудерживающая способность - высокая;
3) испарение с поверхности - низкое.
Этим условиям соответствуют, например, черноземы.
3.2.1.2.3. Кислород и аэрация почвы
Чтобы расти и поглощать биогенные элементы, корням необходима энергия, генерируемая при окислении глюкозы в процессе клеточного дыхания. При этом потребляется кислород и в качестве отхода образуется СО2.
У корней должна быть возможность поглощать О2 из окружающей почвы и удалять в нее СО2. Безусловно, обеспечение диффузии (пассивного движения) кислорода из атмосферы в почву и обратное перемещение СО2 - важнейшая черта почвенной среды. Этот показатель характеризует аэрация.
Аэрация - естественное или искусственное поступление воздуха в какую-либо среду (воду, почву и т.д.). Она может производиться при помощи технических средств или путем ликвидации преграды (льда, масляной пленки и др.), препятствующей естественному доступу воздуха к поверхности воды, почвы.
Аэрацию почвы обычно затрудняют 2 обстоятельства:
1) уплотнение почвы;
2) насыщение её водой.
3.2.1.2.4. Водородный показатель (рН) и кислотность почвы
Кислотность почвы важнейший показатель. Например, фосфаты легче усваиваются растениями в кислых почвах.
Число рН - реальная концентрация ионов водорода [H+], выраженная в единицах водородного показателя:
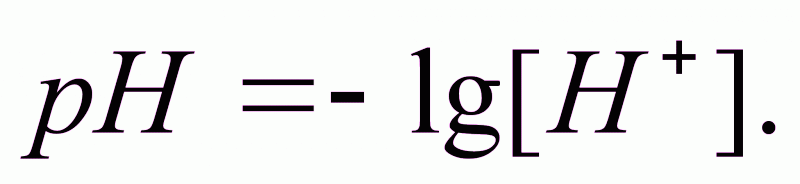
При равной концентрации ионов Н+ и ОН- - среда нейтральная, а рН = 7. Если [H+] больше концентрации гидроксильных ионов [ОH-], то среда кислая, а рН меньше 7. При [ОH-] > [H+] - cреда щелочная, а рН больше 7.
Например, рН = 1 и рН = 14 соответствуют: [H+] = 10-1 моль/л и [H+] = 10-14 моль/л.
3.2.1.2.5. Механический состав почвы и размеры минеральных частиц
Структура и механический состав почвы определяются относительным содержанием в ней песка (размеры его частиц: 0,052 мм) и глины (размером < 0,002 мм). Имеется 11 структурных классов почв. Идеальная почва должна содержать приблизительно равные количества глины и песка с частицами промежуточных размеров. В этом случае образуется пористая, крупитчатая структура, и почва называется суглинками (размер частиц ближе к размерам частиц глины, чем песка). Если же преобладают песчаные частицы, то можно говорить о супесях. По основным почвенным показателям суглинки значительно превосходят глину и песок, что хорошо видно из табл. 3.1.
Таблица 3.1. Сравнительные показатели (характеристики) для различных типов почв
Тип почвы |
Инфильтрация |
Водоудержи- вающая спо- собность |
Ионно- обменная емкость |
Аэрация |
Обрабатываемость |
|
Песок Глина Суглинки |
+++ + ++ |
+ ++++ ++ |
+ ++++ ++ |
+++ - ++ |
+++ - ++ |
3.2.1.3. Почва и глобальные проблемы
3.2.1.3.1. Наиболее опасные воздействия человека на почву
Загрязнение химическим веществами.
Антропогенная эрозия.
Засоление (главным образом, за счет чрезмерного водного орошения).
Заболачивание.
Добыча полезных ископаемых (главным образом - горючих, а также металлических руд).
Использование плодородной почвы под строительство.
3.2.1.3.2. Загрязнения почвы
Главными загрязнителями являются промышленные предприятия (черной и цветной металлургии, энергетики, химической промышленности), вызывающие загрязнение токсичными веществами, включая тяжелые металлы, а также компоненты, способствующие выпадению кислотных дождей. Автотранспорт дает загрязнение свинцом и утечками топлива, быт и строительство (бытовые отходы, свалки), сельское хозяйство (загрязнение пестицидами, а иногда и перенасыщение почвы удобрениями). Значительное загрязнение дают утечки топлива (аварии нефтепроводов, а также при операциях транспортировки), могильники с радиоактивными отходами и токсичными веществами и др. источники.
3.2.1.3.3. Эрозия почвы и опустынивание земель
Эрозия почвы (от лат. erosio - разъедание) - это процесс разрушения верхних наиболее плодородных слоев почвы и подстилающих пород под действием воды, ветра, вследствие хозяйственной деятельности человеческого общества, а также животных, что приводит и к нарушению структуры почвы, а главное - к уменьшению плодородия почвы.
Археологи установили, что упадок многих ранее могущественных цивилизаций был вызван не внешними врагами, а медленным экологическим самоубийством - неспособностью сохранить земельные и водные ресурсы. Например, Северная Африка, некогда снабжавшая зерном Римскую империю, теперь по большей части представляет собой пустыню. Аналогично, ключевым фактором упадка некогда процветающей в Центральной Америке культуры Майя, вероятно, была потеря почвенного плодородия вследствие эрозии.
За последние 25 лет площади сельскохозяйственных угодий сократились на 33 млн га, несмотря на ежегодное вовлечение в сельскохозяйственный оборот новых земель. Подсчитано, что земельные ресурсы на душу населения уменьшаются на 2 % за год, плодородные земли (угодья) на 6-7 %. Русские экологи А.В. Яблоков и С.А. Остроумов (данные 1985 г.) считают, что ежегодно в мире площади пашен и пастбищ под влиянием деятельности человека сокращаются на 5-8 млн га. Из них в результате эрозии теряется примерно 3 млн га, подвергается различным видам опустынивания - 2 млн га и исключается из пользования в результате загрязнения - около 2 млн га. Пустыни интенсивно наступают и занимают все большие территории. Так, отмечен в некоторые годы рост пустыни Сахара со скоростью порядка 48 км в год. Потери почвы в основном вследствие вышеуказанных факторов, а также рост численности населения обусловливают интенсивное уменьшение площади почвы на душу населения. Считается, что в 1950 г в мире на душу населения приходилось 0,24 га пашни, а к 1983 году эта площадь уже уменьшилась до 0,15 га, в России же сейчас на душу населения приходится большая площадь - около 0,9-1 га на человека. Следует, однако, учитывать, что основные площади пахотных земель России расположены в районах с неблагоприятными условиями для земледелия, где имеется недостаток, либо избыток тепла и влаги. Однако вместо того, чтобы усвоить уроки прошлого, мы склонны повторять ошибки в глобальном масштабе. По оценке Института мировой статистики потери почвы от эрозии в мире из года в год продолжают расти. В отличие от землетрясений и извержений вулканов это бедствие надвигается постепенно, но это не уменьшает значения проблемы.
3.2.1.3.3.1. Типы эрозии почвы
Геологическая: а) водная; б) ветровая.
Антропогенная.
Зоогенная (пастбищная).
В водной эрозии в качестве разрушающей силы выступает текущая и падающая вода. Водную эрозию подразделяют на плоскостную (равномерно сносится водными потоками поверхностный слой почвы), струйчатую (заметно проявляются слабые очаги эрозии по местам концентрации водных потоков), бороздчатую и овражную (как следующие две стадии струйчатой, сопровождающиеся очаговым разрушением почв и даже грунтов с выносом больших масс продуктов эрозии в водные источники, из-за этого на 1 га пашни приходится до 5-10 км оврагов), ирригационную (связана с подачей на поверхность больших масс воды, которая не успевает впитываться и стекает по поверхности, а часто сопровождается и засолением почв), капельную (разрушение структуры почв каплями воды, что приводит к ее уплотнению и уменьшению водопроницаемости), русловую (например, действие речных водных потоков), а также подземную (боковую и глубинную) и др.
Ветровая эрозия (или дефляция) - это разрушение почвы за счет движения воздуха (ветра). Она сильно зависит от скорости ветра и его продолжительности, степени от открытости пространства (рельефа, наличия растительности и особенно леса), а также от типа и структуры почвы. Эрозию усиливает сухость почв обеднение их гумусом. Особенно велика опасность ветровой эрозии в степях (характерный пример, освоение у нас целинных земель за Уралом), полупустынях и пустынях.
Антропогенная эрозия (разрушение почвы в результате хозяйственной деятельности человека) включает: механическую и транспортную (вызывает нарушение структуры почвы, например, при использовании тяжелой сельскохозяйственной техники или неверных способах обработки земель), строительную (карьеры, вырубка лесов, строительство на плодородных землях), химическую (загрязнение веществами приводилось выше), пастбищную (вытаптывание и уплотнение почвы животными, обкусывание растений, чрезмерное увеличение детрита в почве из-за длительного выпаса животных на одном месте и др.), а также водную антропогенную (капельная, струйчатая, овражная, ирригационная, которые были рассмотрены выше). При этом особо нужно остановиться на орошаемом земледелии. Сейчас в мире около 250 млн га орошаемых земель, а в России - примерно 6 млн га. При этом кроме ирригационной эрозии поливные почвы часто подвергаются так называемому вторичному засолению. Избыточная влага постепенно проникает до грунтовых вод и обусловливает повышение их уровня. За короткое время грунтовые воды с глубины 20-30 м могут близко подниматься и даже выходить на поверхность почвы. При испарении воды с поверхности растворенные в этих водах соли накапливаются в поверхностном слое почвы. Это и есть вторичное засоление, которое, в частности, можно оценить и по увеличению показателя плотности почвы, ведь ранее указывалось, что плотность черноземов примерно 1,1-1,2 г/см3. Это ведет к уменьшению урожайности почвы и другим неблагоприятным последствиям. Первичное засоление (образование солончаков) происходит естественным порядком без участия человека.
3.2.1.3.3.2. Основные причины ускоренной эрозии
Неверные методы земледелия (введение монокультур, неправильное орошение и обработка почвы);
Перевыпас животных (пастбищная эрозия - рассматривалась выше);
Сведение лесов (леса регулируют поверхностный и подземный сток, химический состав почвы - наличие солей и детрита, определяют климатические условия, включая воздействие ветра).
3.2.1.3.3.3. Предупреждение эрозии почвы
С этой целью проводятся зональные и межзональные мероприятия, включающие: агротехнические, гидротехнические и организационно-хозяйственные. Примеры: соблюдение севооборотов (пропашные культуры, например, кукуруза, картофель, должны сменяться посевами, скрепляющими почву корнями, например травосмесями), проведение контурной вспашки (по горизонталям рельефа), использование техники с малым удельным давлением на почву, создание полезащитных полос, разумная химизация (биологическая защита культур вместо использования пестицидов, селекция) и орошение земель, умеренные нагрузки в агроэкосистемах, регулирование выпаса животных и другие направления.
В заключение необходимо отметить, что самоочистка и естественное восстановление почвенного покрова на нашей планете протекают очень медленно по сравнению с самоочисткой атмосферы и гидросферы.
3.2.2. Главные направления защиты земельного фонда
Максимально полное и комплексное извлечение всех полезных компонентов из природных месторождений (меньше отходов, отвалов);
Экономное использование сырья и топлива;
Разработка экологически чистых источников энергии;
Глубокая очистка отходов от токсичных веществ;
Разработка безотходных технологий и создание предприятий, работающих по замкнутому циклу (например, из навоза получают биогаз);
Воссоздание лесов;
Рациональное использование сельскохозяйственных земель;
Рекультивация (восстановление и повторное использование земель в местах добычи полезных ископаемых).
3.3. Атмосфера Земли и глобальные проблемы
3.3.1. Общая характеристика атмосферы
Атмосфера - внешняя, газоподобная оболочка планеты, которая, с одной стороны, непосредственно прилегает к земной поверхности, а, с другой стороны, постепенно переходит в космический вакуум.
Важнейшие функции атмосферы:
она является необходимым источником, обеспечивающим жизнь в биосфере (определяет климат на планете, ускоряет процессы кругооборота веществ и самоочистки в биосфере и др.);
подобно “чехлу” защищает живые организмы на нашей планете от пагубного влияния космического излучения.
Масса атмосферы составляет около 5,91015 т.
3.3.2. Строение атмосферы
Атмосфера имеет слоистое строение, то есть состоит из нескольких сфер, между которыми располагаются переходные слои - паузы. В сферах изменяется химический состав, температура и давление.
3.3.2.1. Тропосфера и состав воздуха
Наиболее плотный слой воздуха, прилегающий к земной поверхности, - это тропосфера. Толщина ее изменяется так: в средних широтах (до 10-14 км) над уровнем моря, на полюсах - (до 7-10 км), над экватором - (до 16-18 км). При этом среднее значение (примерно 11-13 км). Масса тропосферы составляет 4/5 от всей массы атмосферы. Средний состав атмосферного воздуха представлен в табл.3.2.
Таблица 3.2. Состав сухого атмосферного воздуха у земной поверхности
| Компоненты | Содержание, в объем. % | Компоненты | Содержание, в объем. % |
|
Азот ( N2 ) |
78,09 | Оксид азота ( NO ) |
2,510-4 |
|
Кислород ( О2 ) |
20,94 |
Метан ( СН4 ) |
1,510-4 |
| Аргон ( Ar ) | 0,93 |
Диоксид азота ( NO2 ) |
1,510-4 |
|
Углекислый газ (СО2) |
О,034-0,035 |
Диоксид серы ( SO2 ) |
110-4 |
| Неон ( Ne ) |
1,810-3 |
Водород ( Н2 ) |
510-5 |
| Гелий ( Не ) |
5,210-4 |
Угарный газ ( СО ) |
10-5 |
| Криптон ( Kr ) |
110-4 |
Озон ( О3 ) |
210-6 |
| Ксенон ( Хе ) |
810-6 |
Аммиак ( NH3 ) |
10-6 |
Другие составляющие воздуха: водяной пар, пыль, сажа и иные загрязнители, включая антропогенные. Наиболее в широких пределах изменяется содержание в воздухе водяного пара и пыли, что зависит от множества причин. При этом содержание водяного пара значительно убывает с высотой от поверхности Земли. В результате испарения воды с земной поверхности (особенно с Мирового океана) и в результате процессов конденсации образуются облака и затем выпадают осадки. Большая часть облачности присутствует в тропосфере (особенно на высоте до 1,5-2,5 км от поверхности Земли). Примерно 50 % всей земной поверхности закрыто облаками. Главный источник тепла на Земле - солнечная энергия, но тропосфера в основном нагревается от Земли (отдается накопленная энергия). При этом нельзя не учитывать процессы рассеивания солнечной энергии, а также задержку тепла в приземном слое особенно из-за антропогенных выбросов СО2, создающих парниковый эффект, что в целом приводит к увеличению доли инфракрасного (теплового) излучения в тропосфере. Температура же в приземном слое колеблется в пределах примерно от (+500С) до (-500С). В целом с удалением от поверхности Земли температура в пределах тропосферы уменьшается примерно на 0,5-0,6 градуса на каждые 100 метров. С высотой разряжение воздуха возрастает, а атмосферное давление уменьшается. Ветровые потоки в тропосфере очень разнообразны.
Выше тропосферы находится тропопауза (так, тропическая на высоте 16-18 км, а полярная на высоте 9-10 км от земной поверхности). В тропопаузе нет столь разнообразных ветровых потоков как в тропосфере и температура практически постоянна. Тропопауза как бы защищает биосферу от чрезмерных потерь тепла в космическое пространство.
3.3.2.2. Стратосфера и защитный “озонный слой”
В следующем слое (стратосфере) с высотой концентрация воздуха в целом продолжает уменьшаться, но при этом начинает увеличиваться концентрация озона О3 (это так называемый “озонный экран”), который располагается у полюсов с высоты примерно 9 км, а у экватора – на расстоянии 18 км от земной поверхности. Максимума содержание озона достигает приблизительно на высоте 22-25 км (концентрация озона уровня 0,01-0,06 мг/м3, то есть на несколько порядков выше, чем в тропосфере). Однако, если содержащийся в границах экрана озон выделить в чистом виде, то слой его составит 3-5 мм. Содержание озона выражается в сантиметрах (0,3-0,5) или в единицах Допсона (миллиметры, увеличенные в 100 раз - 300-500 ед.). Из-за наличия “озонного экрана” стратосферу часто называют озоносферой. Главная роль стратосферы (благодаря “озонному экрану”) - это защита биосферы от жесткого ультрафиолетового излучения.
В 1930 году английский геофизик С. Чепмен для объяснения постоянной концентрации озона в стратосфере предложил схему (из четырех реакций), известную нам сейчас под названием - цикл Чепмена:
h
О2 2О (при действии ультрафиолетового излучения с 242 мкм);
О + О2 + М О3 + М;
О + О3 + К 2 О2 + К;
h
4) О3 О2 + О (защита от ультрафиолетового излучения, происходит поглощение в области = 240-320 мкм).
Первая и четвертая реакции по механизму - фотохимические (протекают под действием солнечной радиации), вторая и особенно третья реакции по механизму - каталитические. Так, в третьей реакции роль катализатора К может выполнять оксид азота NO, который образуется под действием жесткого солнечного излучения, а также при грозовых разрядах и при антропогенных выбросах (например, выбросы из двигателей реактивных самолетов в стратосфере). Упрощенно механизм катализа может быть представлен следующими реакциями:
О3 + NO NO2 + O2
NO2 + O NO + O2,
то есть концентрация оксида азота NO не меняется, а концентрация озона О3 снижается.
В стратосфере имеется облачность, хотя в сравнении с тропосферой она незначительна. Протяженность стратосферы (в среднем до высоты 45 км от поверхности Земли). Температура в пределах этого слоя сначала несколько уменьшается, но с высоты 22-25 км (где значительная концентрация озона) начинает увеличиваться и на верхней границе стратосферы близка 00С. Причина этого, по мнению климатологов, в том, что в результате поглощения ультрафиолетового излучения “озоновым экраном” происходит преобразование лучей в инфракрасные тепловые.
В стратопаузе, имеющей несколько большую протяженность, чем тропопауза, температура изменяется незначительно. Верхняя граница стратопаузы находится на высоте порядка 50 км от земной поверхности. Стратопауза выполняет защитную функцию от ионизационного излучения.
3.3.2.3. Характеристика мезосферы, ионосферы и экзосферы
Третий слой атмосферы - мезосфера (средняя атмосфера) заканчивается на высоте приблизительно 80 км от земной поверхности. Характеризуется значительной разряженностью воздуха и резким уменьшением содержания озона (в сравнении со стратосферой). Это последний слой, где еще присутствует незначительная облачность. В этом слое температура уменьшается (например, на высоте 80 км от земной поверхности температура отрицательная - 700С). Мезопауза находится от земной поверхности на высоте 80-100 км - это граница плотных слоев атмосферы.
Выше располагается следующий слой - термосфера (или ионосфера). Это слой с высоким разрежением “воздуха” и характеризуется постоянным ростом температуры с высотой, хотя из-за высокого разрежения сведения об уровне температуры противоречивы. Приводятся такие данные: на высоте 150 км (t0 = 200-2400C), 500-600 км (свыше 15000С). Под действием солнечного излучения молекулы ионизированы (например, N-, O-, O2-, NO2-, NO3-, H+, N+, O+, O2+ и др.) и движутся с большими скоростями. На высоте 110-120 км уже нет молекулярного кислорода, но есть атомарный или ионизированный. Выше 400-500 км от земной поверхности все газы находятся в атомарном или ионном состояниях. Кислород и азот преобладают до высоты 400-600 км, т.к. выше 600 км начинает преобладать гелий (“гелиевая корона”). В ионосфере имеется высокая концентрация электронов. Этот слой достаточно протяженный и завершается на высоте 800 км от земной поверхности. Именно в этом слое находятся спутники, пребывают космические станции. Одна из защитных функций ионосферы - например, защита биосферы от рентгеновского космического излучения.
Последний слой атмосферы (недостаточно изученный) - экзосфера (“внешняя атмосфера”). Данные по ее протяженности противоречивы. Так, называется верхняя граница (высота 1600 км от земной поверхности, а по другим данным - на тысячи км больше, возможно, этот слой то сжимается, то расширяется на тысячи км). По одним данным, на высотах от земной поверхности от 600 до 1600 км преобладает гелий (этот промежуток известен под названием “гелиевая корона”). По другим данным, с высоты от 1000 км располагается протоносфера (весь водород в атомарном виде) с примесью гелия. По другим данным, водород начинает преобладать на высоте 2000-3000 км. Экзосфера выполняет роль защитного экрана от электронов высоких энергий.
Выше экзосферы расположена магнитосфера (пространство выше атмосферы, где формируется магнитное поле Земли). Она защищает биосферу от солнечной плазмы, содержащей частицы с высокими энергиями.
3.3.3. Загрязнение атмосферы
Имеется два главных источника загрязнения атмосферы: естественный и антропогенный. К естественному относятся:
вулканические, сейсмические процессы (извержения вулканов, деятельность фумарол и гейзеров, загрязнения при землетрясениях), основными компонентами которых являются: пыль, пепел, диоксид серы, сероводород, оксиды углерода и азота, HF и другие вещества;
пылевые бури, ураганы, смерчи и процессы активного выветривания горных пород, вызывающие загрязнение пылью размером частиц 10-3 - 10-4 см органического (споры грибов, пыльца растений и др.) и неорганического происхождения. Особенно активное запыление воздуха происходит в пустынях и степях. Однако атмосферная пыль до определенного уровня по содержанию в воздухе имеет и большое значение. Она способствует конденсации водяных паров, а значит, и образованию осадков, а также поглощает прямую солнечную радиацию (вызывает снижение температуры в приземном слое);
лесные пожары из-за грозовых разрядов (молнии) и вулканических процессов, приводящих к загрязнению оксидами, углеводородами и другими органическими веществами, пепелом.
процессы разложения, гниения вследствие деятельности бактерий и других организмов в почве, природных водоемах (особенно болотах) и др.;
космическая пыль (ежегодно на уровне 2-5 млн т);
временные загрязнения (особенно над океанами) мельчайшими кристалликами солей натрия, кальция, магния, аэрозолями и др.
К антропогенным источникам загрязнения атмосферы относятся: теплоэнергетика; металлургия; транспорт (особенно авто- и авиатранспорт); химическая промышленность; горнодобывающая отрасль производства; строительство; бытовая сфера; военные испытания и войны; антропогенные катастрофы (пожары, ядерные взрывы, аварии на промышленных предприятиях, а также при транспортировке летучих токсичных веществ).
При этом главными антропогенными загрязнителями атмосферы являются: оксиды углерода, серы и азота; пыль (включая частицы металлов), аэрозоли; углеводороды, их производные и другие органические летучие вещества; галогены и их производные; радиоактивные компоненты; сероводород; аммиак.
Важнейшими свойствами атмосферы является ее способность к быстрому перемешиванию и перемещению больших масс воздуха на большие расстояния, а также связь с другими сферами и особенно с океаном (так, океан поглощает значительную долю антропогенных выбросов углекислого и сернистого газов). Загрязненность воздуха в городах в среднем в 15 раз выше, чем в сельской местности, и в 150 раз выше, чем над океаном. С одной стороны, атмосферный воздух активно переносит (за счет ветровых потоков) значительные массы загрязняющих веществ, что порой приводит к катастрофическому загрязнению почвы и водоемов в местах достаточно удаленных от места антропогенных выбросов (например, сжигание бурого угля в Англии, Германии и Люксембурге часто вызывало выпадение кислотных дождей в Скандинавских странах). С другой стороны, атмосфера (в отличие от гидросферы и особенно почвы) имеет высокую способность к самоочищению. Значительную роль в очистке атмосферы от загрязняющих играют также леса и выпадение осадков.
3.3.4. Глобальные проблемы атмосферы
Известны такие глобальные проблемы, непосредственно связанные с атмосферой, как парниковый эффект, разрушение озонового слоя в стратосфере, смог и кислотные дожди. Рассмотрим их. Влияние различных антропогенных загрязнителей на некоторые глобальные проблемы биосферы приведено в табл. 3.3.
3.3.4.1. Парниковый эффект
Парниковый эффект, главным образом, реализуется, за счет увеличения сжигания углеродного топлива и постоянного роста антропогенных выбросов СО2 в атмосферу. Наибольший уровень этих выбросов приходится на теплоэнергетику (деятельность ТЭС). Данные приблизительно за последние 150 лет неутешительны. Содержание углекислого газа в атмосфере постоянно увеличивается (данные в объем.%): в 1860 г. - 0,028, в 1900 г. - 0,029, в 1950 г. - 0,030, в 1992 г. - 0,032, а в 2000 г. (по разным данным) - примерно 0,034-0,035.
Сейчас увеличение концентрации СО2 идет примерно со скоростью 0,3-0,5 % за год. Суть парникового эффекта состоит в следующем: при сжигании органического топлива происходят выбросы газообразных веществ: доля углекислого газа составляет от 50 до 65 %, метана (около 20 %), оксидов азота (5 %), озона, фреонов, водяных паров и других газов (около 10-25 % парникового эффекта). Эти компоненты образуют “газообразный шар” вокруг планеты, препятствующий отдаче тепла в космическое пространство (то есть выполняют роль “тепловой ловушки”), хотя и не препятствует проникновению солнечной радиации к поверхности Земли. В результате этого среднегодовая температура постепенно увеличивается на десятые доли градуса, а это, в свою очередь, вызывает таяние льдов на полюсах планеты, так что постепенно приводит к поднятию уровня Мирового океана, затоплению ряда островов и прибрежных территорий материков, и, наконец, к климатическим изменениям. Последствия таких процессов - это засуха в некоторых регионах и опустынивание земель (пример тому - Африка), природные катаклизмы (например, ураганы, смерчи, тайфуны, наводнения).
За счет парниковых газов (табл.3.3) температура в приземном слое за последнее столетие повысилась на 0,3-0,6 0С. Если и дальше будет увеличиваться содержание СО2 в атмосфере, то по прогнозам к 2050 г. оно может достигнуть 0,064 объем. %, что (по данным разных научных источников) обусловит повышение среднегодовой температуры планеты на 1-3,5 0С. Это, в свою очередь, вызовет дополнительное таяние ледников и подъем уровня океана примерно на 1,5 м (за столетие он повысился на 10-12 см), что вызовет затопление около 5 млн км3 суши и катастрофические климатические изменения. Климатологи крайне опасным считают выброс порядка 15-20 млрд т СО2 за год (полная экологическая катастрофа), к концу ХХ столетия же выбросы составляли 6,5-7 млрд т СО2 за год. Опасность глобального нарушения равновесия в биосфере также еще связана с массовой вырубкой леса и загрязнением Мирового океана, которые являются главными “утилизаторами” углекислого газа. С 70-х годов ХХ столетия неоднократно проводились Международные форумы и конференции (одна из первых - в Торонто в 1979 г.), где говорилось об ограничении выбросов парниковых газов. В 90-е годы в Японии был подписан Киотский протокол об уменьшении этих выбросов развитыми странами на 8 % к 2010 г. Под этим документом были поставлены подписи представителей ведущих мировых держав, которые и выбрасывают в атмосферу большую часть парниковых газов. Однако с приходом к власти в США нового президента Буша в 2001 г. последовало заявление американской администрации об отказе выполнения Киотского документа, что грозит миру опасными непредсказуемыми последствиями.
Таблица 3.3. Антропогенные загрязнители и обусловленные ими изменения в атмосфере (по данным Вронского, 1996 г. и др. авторов)
Антропогенные загрязнители атмосферного воздуха |
Изменения в атмосфере под влиянием загрязнителей (“+” усиление, “-” ослабление, * слабое усиление) |
|||||
|
Парни- ковый эффект |
Разру-шение озонного слоя |
Кислот- ные дожди |
Фото- хими- ческий смог |
Прозрач- ность атмо-сферы |
Само- очищение атмосферы |
|
| Оксид углерода (СО) | | |||||
|
Углекислый газ (СО2) |
+ | * | ||||
|
Диоксид серы (SO2) |
+ | | ||||
|
Метан (СН4) |
+ | |||||
|
Оксиды азота: NO, NO2 и др. |
+ | + | + | + | | |
|
Фреоны (CCl2F2 и др.) |
+ | + | ||||
|
Озон (О3) |
+ | + | + | |||
| Альдегиды | + | |||||
| Пыль | | |||||
Глобальные проблемы истощения озонного слоя в стратосфере, смога и кислотных дождей подробно рассматривались в разделе «Глобальная экология».

