 РЕЗЕРФОРД
Эрнст (1871-1937), английский физик, один из создателей учения о
радиоактивности и строении атома, основатель научной школы, иностранный
член-корреспондент РАН (1922) и почетный член АН СССР (1925). Директор
Кавендишской лаборатории (с 1919). Открыл (1899) альфа- и бета-лучи и установил
их природу. Создал (1903, совместно с Ф. Содди) теорию радиоактивности.
Предложил (1911) планетарную модель атома. Осуществил (1919) первую
искусственную ядерную реакцию. Предсказал (1921) существование нейтрона.
Нобелевская премия (1908).
РЕЗЕРФОРД
Эрнст (1871-1937), английский физик, один из создателей учения о
радиоактивности и строении атома, основатель научной школы, иностранный
член-корреспондент РАН (1922) и почетный член АН СССР (1925). Директор
Кавендишской лаборатории (с 1919). Открыл (1899) альфа- и бета-лучи и установил
их природу. Создал (1903, совместно с Ф. Содди) теорию радиоактивности.
Предложил (1911) планетарную модель атома. Осуществил (1919) первую
искусственную ядерную реакцию. Предсказал (1921) существование нейтрона.
Нобелевская премия (1908).
Опыт Резерфорда (1906
г.) по рассеянию быстрых заряженных частиц при прохождении через тонкие слои
вещества позволили исследовать внутреннюю структуру атомов. В этих опытах для
зондирования атомов использовались α – частица – полностью ионизированные
атомы гелия, - возникающие при радиоактивном распаде радия и некоторых других
элементов. Этими частицами Резерфорд бомбардировал атомы тяжелых металлов.
Резерфорду было известно, что атомы состоят из
легких отрицательно заряженных частиц – электронов и тяжелой положительно
заряженной частицы. Основная цель опытов – выяснить, как распределен
положительный заряд внутри атома. Рассеяние α – частиц (то есть изменение
направления движения) может вызвать только положительно заряженная часть атома.
Опыты показали, что
некоторая часть α – частиц рассеивается на большие углы, близки к
180˚, то есть отбрасывается назад. Это возможно только в том случае, если
положительный заряд атома сосредоточен в очень малой центральной части атома –
атомном ядре. В ядре сосредоточена также почти вся масса атома.
Оказалось, что ядра
различных атомов имеют диаметры порядка 10-14 – 10-15 см,
в то время как размер самого атома ≈10-8 см, то есть в 104
– 105 раз превышает размер ядра.
Таким образом, атом
оказался «пустым».
На основании опытов
по рассеянию α – частиц на ядрах атомов Резерфорд пришел к планетарной
модели атома. Согласно этой модели атом состоит из небольшого положительно
заряженного ядра и обращающихся вокруг него электронов.
С точки зрения
классической физики такой атом должен быть неустойчив, так как электроны
движущиеся по орбитам с ускорением, должны непрерывно излучать электромагнитную
энергию.
Дальнейшее развитие
представлений о строении атомов было сделано Н. Бором (1913 г.) на основе
квантовых представлений.
Лабораторная работа.
Данный опыт возможно провести при помощи
специального прибора, чертеж которого изображен на рисунке 1. Этот прибор
представляет собой свинцовую коробочку с полным вакуумом внутри её и
микроскопом.
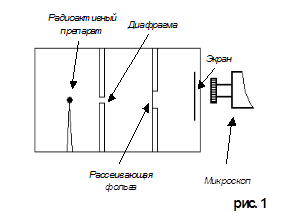
Рассеяние
(изменение направления движения) α – частиц может вызвать только
положительно заряженная часть атома. Таким образом, по рассеянию α –
частиц можно определить характер распределения положительного заряда и массы
внутри атома. Схема опытов Резерфорда показана на рисунке 1. Испускаемый
радиоактивным препаратом пучок α – частиц выделялся диафрагмой и после
этого падал на тонкую фольгу из исследуемого материала (в данном случае это
золото). После рассеяния α – частицы попадали на экран, покрытый сернистым
цинком. Столкновение каждой частицы с экраном сопровождалось вспышкой света
(сцинтилляцией), которую можно было наблюдать в микроскоп.
При хорошем вакууме
внутри прибора в отсутствие фольги на экране возникала полоска света, состоящая
из сцинтилляций, вызванных тонким пучком α – частиц. Но когда на пути
пучка помещалась фольга, α – частицы из-за рассеяния распределялись на
большей площади экрана.
В нашем опыте нужно
исследовать α – частицу, которая направлена на ядро золота при составлении
угла 180° (рис. 2) и проследить за реакцией α – частицы, т.е. на какое
минимальное расстояние α – частица приблизится к ядру золота (рис. 3).
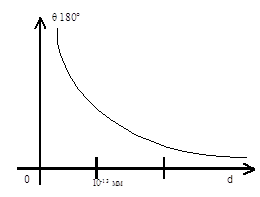 Рис. 2
Рис. 2
 Рис.3
Рис.3
Дано:
V0=1,6*107 м/с
– начальная скорость
d = 10-13
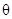 = 180°
= 180°
rmin=?
Вопрс:
Какое минимальное расстояние rmin
между α – частицей и ядром удастся реализовать в данном эксперименте?
(Рис. 4)
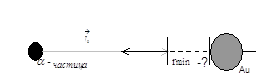 Рис.4
Рис.4
Решение:
В нашем эксперименте α – частица представлена как
атом 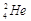
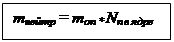 mнейтр
mнейтр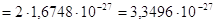 кг
кг
Z=2 – протонов
N = Au
– Z = 4 – 2 = 2 нейтрона
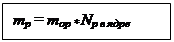
mp=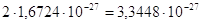 кг
кг
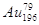 Z=79 – число протонов
Z=79 – число протонов
N = Au
– Z = 196 – 79 =117 (нейтронов)
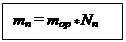
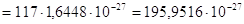 кг
кг
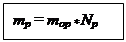
 кг
кг
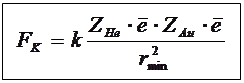

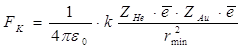
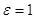
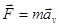
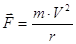
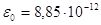 Кл2/H ∙м2 – электрическая постоянная
Кл2/H ∙м2 – электрическая постоянная
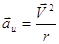
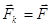
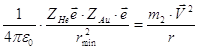 m2=6,6∙10-27кг
m2=6,6∙10-27кг
ZHe∙2∙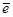 — заряд ядра (He) ZAu∙
— заряд ядра (He) ZAu∙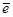 — заряд ядра (Au)
— заряд ядра (Au)
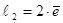 — заряд
α-частицы равен 2 элементарным.
— заряд
α-частицы равен 2 элементарным.
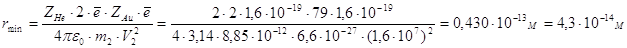
Ответ: rmin=4,3·10-14
м
Вывод: При этом
опыте удалось выяснить, что a-частица смогла
приблизится к ядру атома на минимальное расстояние, которое составило rmin=4,3·10-14 м и возвратится
обратно, по той же траектории по которой она начинала движение.
Когда этот же опыт
Резерфорд проделал в первые, при таком расположении a-частицы
по отношению к углу составляющему 180° он удивленно сказал: «Это почти столь
же невероятно, как если бы вы выстрелили 15-дюймовым снарядом в кусок тонкой
бумаги, а снаряд возвратился бы к вам и нанес вам удар».
И в правду, это не
вероятно, дело в том, что проводя этот опыт на меньших углах, то а - частица
обязательно отскочит в сторону, подобно тому как камушек несколько десятков
граммов при столкновении с автомобилем не в состоянии заметно изменить его
скорость (рис. 5). Так как их масса примерно в 8000 раз больше массы электрона,
а положительный заряд равен по модулю удвоенному заряду электрона. Это не что
иное, как полностью ионизированные атомы гелия. Скорость α – частиц очень
велика: она составляет 1/15 скорости света.
Следовательно, электроны вследствие своей малой массы не могут заметно изменить
траекторию α – частицы.
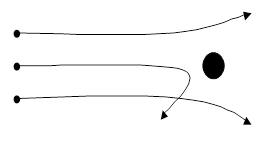 Рис. 5
Рис. 5
Другие работы по теме:
Билеты по Физике
Вопросы к экзамену по Физике Электрический ток в электролитах. Законы электролиза. Электропроводимость газов. Самостоятельный и несамостоятельный газовые разряды.
Опыт Резерфорда
ЕЗЕРФОРД Эрнст (1871-1937), английский физик, один из создателей учения о радиоактивности и строении атома, основатель научной школы, иностранный член-корреспондент РАН (1922) и почетный член АН СССР (1925). Директор Кавендишской лаборатории (с 1919). Открыл (1899) альфа- и бета-лучи и установил их природу.
Распределение Ландау
Порядок и основные этапы взаимодействия электронов с веществом. Процесс рассеяния электронов, отличительные признаки упругих и неупругих столкновений. Метод Монте-Карло в задачах переноса частиц в веществе. Этапы алгоритма решения поставленной задачи.
Квантовая теория атома
Классическая модель строения атома. Понятие орбиты электрона. Набор возможных дискретных частот. Водородоподобные системы по Бору. Недостатки теории Бора. Значение квантовых чисел. Спектр излучения атомов. Ширина спектральных линий. Доплеровское уширение.
Английский физик Эрнест Резерфорд
Изучение атомной структуры. Теория радиоактивности. Получение Нобелевской премии. Новая модель атома. Председатель правительственного консультативного совета Управления научных и промышленных исследований. Общественная деятельнось.
Революция в естествознании
Доклад по истории Ученика 9 «Д» класса Лицея №88 Фельдмана Виталия. Революция в естествознании. В начале XX века сложились все условия для мощного прорыва, скачка, революции в естествознании, а особенно в физике. Однако в той или иной степени это отразилось и на других естественных науках, например на химии.
Примерные экзаменационные билеты по физике (11 класс)
Примерные экзаменационные билеты по физике Билет №1 Механическое движение. Относительность движения. Система отсчета. Материальная точка. Траектория. Путь и перемещение. Мгновенная скорость. Ускорение. Равномерное и равноускоренное движение.
П.Л. Капица
Старый Петергоф 1998 год Выбирая тему для реферата, мне не столько хотелось описать историю какого-нибудь открытия или выдающиеся работы, проделанные определенным человеком, сколько «открыть» для себя и быть может для других знаменитую личность с человеческой стороны.
Опыты Резерфорда
МИНИСТЕРСТВО ВЫСШЕГО И СРЕДНЕГО СПЕЦИАЛЬНОГО ОБРАЗОВАНИЯ РФ. НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ АРХИТЕКТУРНО-СТРОИТЕЛЬНЫЙ УНИВЕРСИТЕТ кафедра физики
Теория столкновений
Изучение процессов рассеяния заряженных и незаряженных частиц как один из основных экспериментальных методов исследования строения атомов, атомных ядер и элементарных частиц. Борновское приближение и формула Резерфорда. Фазовая теория рассеяния.
Примерные экзаменационные билеты по физике 11 класс
Примерные экзаменационные билеты по физике Билет №1 Механическое движение. Относительность движения. Система отсчета. Материальная точка. Траектория. Путь и перемещение. Мгновенная скорость. Ускорение. Равномерное и равноускоренное движение.
Развитие теории атома
Решающим моментом в развитии теории строения атома было открытие электрона. Наличие в электрически нейтральном атоме отрицательно заряженной частицы побуждало предполагать наличие частицы с положительным зарядом. Модель Д. Томсона внесла огромный вклад в экспериментальное изучение строения атома, он стремился найти модель, которая позволила бы объяснить все его известные свойства.
Атомное ядро
Реферат по физике на тему: “Атомное ядро” Москва 1996 Оглавление 1 История открытий в области строения атомного ядра 3 1.1 Модели атома до Бора 3
Модель ядра атома и таблица элементов
Каждый последующий элемент отличается от предыдущего тем, что в его ядре количество протонов увеличивается на единицу, а количество нейтронов растет, в общем случае на несколько.
Атом Бора
Когда Джон Дальтон впервые в истории современной науки предложил атомную теорию строения вещества, атомы представлялись ему неделимыми, наподобие микроскопических бильярдных шаров.
Мое отношение к приметам
Автор: Сочинения на свободную тему Поднимая вопрос, «верить ли в народные приметы?», имеет смысл вспомнить одно из знаменитых изречений китайского философа Конфуция: «Жизненный опыт, - это всего лишь маленький фонарик, не освещающий ничего, кроме пройденного пути». Если философ прав, и жизненный опыт – это, действительно, ничто, то вера в народные приметы должна иметь тот же статус.
Жизнь и робота Нильса Бора
Как метко заметил знаменитый советский ученый П. Л. Капица: «Во всей мировой науке в наши дни не было человека с таким влиянием на естествознание, как Бор. Из всех теоретических троп тропа Бора была самой значительной».
Генри Кавендиш (1731-1810)
Одна из наиболее эксцентрических фигур в истории науки – ). Он был богатым аристократом и состоял в родстве с герцогами Девонширскими. Современники отзывались о нем как о «самом мудрым из богачей и самым богатым из мудрецов».
ГИА физика 2010 кодификатор
Государственная (итоговая) аттестация 2010 года (в новой форме) по ФИЗИКЕ обучающихся, освоивших основные общеобразовательные программы Кодификатор
ГИА физика 2009 кодификатор
Государственная (итоговая) аттестация выпускников IX классов общеобразовательных учреждений 2009 г. (в новой форме) по ФИЗИКЕ Кодификатор элементов содержания по физике
Нильс Хенрик Давид Бор
Нильс Бор - выдающийся датский физик, лауреат Нобелевской премии. Его научные работы, в основном, относятся к теоретической физике, но благодаря им появились новые направления развития химии.
Планетарная модель по Нильсу Бору
Бо́ровская моде́ль а́тома (Моде́ль Бо́ра) — полуклассическая модель атома, предложенная Нильсом Бором в 1913 г. За основу он взял планетарную модель атома, выдвинутую Резерфордом. Однако, с точки зрения классической электродинамики, электрон в модели Резерфорда, двигаясь вокруг ядра, должен был бы излучать непрерывно, и очень быстро, потеряв энергию, упасть на ядро.
Планетарная модель атома
Московский государственный университет Экономики Статистики Информатики Реферат по дисциплине: «КСЕ» на тему «Планетарная модель атома» Выполнил:
Уильям Брэгг
Брэгг, Уильям Лоренс (Bragg, William Lawrence) (1890–1971), английский физик, сын Уильяма Генри Брэгга, удостоенный вместе с отцом Нобелевской премии 1915.
Уильям Рамзай (Рэмзи)
Шотландский химик Уильям Рамзай (Рэмзи) родился в Глазго. Его родителями были инженер и бизнесмен Уильям Рамзай и Катерина (Робертсон) Рамзай, дочь эдинбургского врача, который написал учебник химии.
Нильс Бор
Датский ученый, один из создателей современной физики. Автор основополагающих трудов по квантовой механике, теории атома, атомного ядра, ядерным реакциям.
Сучасна модель атома
Інститут управління природними ресурсами Кафедра фундаментальних наук Реферат з концепції сучасного природознавства на тему: Сучасна модель атома
Модель атома Резерфорда і Бора
Інститут управління природними ресурсами Кафедра фундаментальних дисциплын Реферат з концепції сучасного природознавства на тему: Модель атома Резерфорда і Бора
Концепції фізики атомних і ядерних процесів
а) Моделі атома Вирішальним моментом у розвитку теорії будови атома було відкриття електрона. Наявність у електрично нейтральному атомі негативно зарядженої частинки спонукало припускати наявність частинки з позитивним зарядом. Модель Д.Томсона, не будучи в стані пояснити характер атомних спектрів, що випромінюються атомами, поступилася місцем планетарної моделі Е.Резерфорда.
 РЕЗЕРФОРД
Эрнст (1871-1937), английский физик, один из создателей учения о
радиоактивности и строении атома, основатель научной школы, иностранный
член-корреспондент РАН (1922) и почетный член АН СССР (1925). Директор
Кавендишской лаборатории (с 1919). Открыл (1899) альфа- и бета-лучи и установил
их природу. Создал (1903, совместно с Ф. Содди) теорию радиоактивности.
Предложил (1911) планетарную модель атома. Осуществил (1919) первую
искусственную ядерную реакцию. Предсказал (1921) существование нейтрона.
Нобелевская премия (1908).
РЕЗЕРФОРД
Эрнст (1871-1937), английский физик, один из создателей учения о
радиоактивности и строении атома, основатель научной школы, иностранный
член-корреспондент РАН (1922) и почетный член АН СССР (1925). Директор
Кавендишской лаборатории (с 1919). Открыл (1899) альфа- и бета-лучи и установил
их природу. Создал (1903, совместно с Ф. Содди) теорию радиоактивности.
Предложил (1911) планетарную модель атома. Осуществил (1919) первую
искусственную ядерную реакцию. Предсказал (1921) существование нейтрона.
Нобелевская премия (1908).
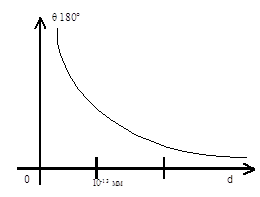 Рис. 2
Рис. 2 Рис.3
Рис.3![]() = 180°
= 180°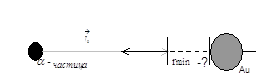 Рис.4
Рис.4![]()
![]() mнейтр
mнейтр![]() кг
кг![]()
![]() кг
кг![]() Z=79 – число протонов
Z=79 – число протонов ![]()
![]() кг
кг![]()
![]() кг
кг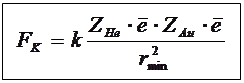
![]()
![]()
![]()
![]()
![]()
![]() Кл2/H ∙м2 – электрическая постоянная
Кл2/H ∙м2 – электрическая постоянная![]()
![]()
![]() m2=6,6∙10-27кг
m2=6,6∙10-27кг![]() — заряд ядра (He) ZAu∙
— заряд ядра (He) ZAu∙![]() — заряд ядра (Au)
— заряд ядра (Au)![]() — заряд
α-частицы равен 2 элементарным.
— заряд
α-частицы равен 2 элементарным.![]()
 Рис. 5
Рис. 5
